2H2O – это химическая формула, которая используется для обозначения молекулы воды. Число "2" перед формулой означает, что в реакциях участвует две молекулы H2O. Как известно, вода состоит из двух атомов водорода (H) и одного атома кислорода (O), поэтому молекула воды изображается как H2O.
2H2O может быть использована для обозначения различных реакций, в которых участвуют молекулы воды. Например, при нагревании воды происходит реакция диссоциации, в результате которой образуются молекулы воды и водорода. Уравнение для этой реакции будет выглядеть следующим образом:
2H2O ⇌ 2H2 + O2
Также 2H2O может быть использована для обозначения реакции окисления воды. В этом случае молекулы воды окисляются при отдаче электронов, и образуются молекулы кислорода (O2) и ионов водорода (H+):
2H2O → O2 + 4H+ + 4e-
Использование формулы 2H2O в химических уравнениях помогает ученым объяснять и предсказывать химические реакции, связанные с молекулами воды. Это позволяет изучать взаимодействие воды с другими веществами и применять полученные знания в различных научных и промышленных областях.
H2O в химии: объяснение и примеры реакций
Наличие атомов водорода и кислорода в молекуле воды делает ее поларной. Это означает, что электроны молекулы неравномерно распределены, создавая разницу в заряде между атомами. В результате вода обладает дипольным моментом и способна образовывать водородные связи с другими молекулами воды или другими веществами.
Вода встречается в различных состояниях: жидком, твердом (лед) и газообразном (пар). Ее свойства и реакции зависят от условий, в которых она находится. Например, при низких температурах вода замораживается, становясь льдом, а при высоких температурах она превращается в пар.
Вода также является растворителем для многих веществ. Она способна растворять множество ионов, молекул и соединений, делая их доступными для химических реакций. Это свойство играет важную роль в биологических системах, так как большинство реакций в организмах происходят в водной среде.
Примеры реакций, в которых участвует H2O, включают гидролиз, окислительно-восстановительные реакции и фотосинтез. Гидролиз - это реакция, при которой вода разлагается на ионы водорода (H+) и гидроксиды (OH-). Окислительно-восстановительные реакции - это реакции, в которых H2O может служить как окислителем (получая электроны) или восстановителем (отдавая электроны). Фотосинтез - это процесс, в котором H2O превращается в кислород с помощью энергии от солнечного света, что является ключевым шагом в процессе поглощения света растениями.
| Реакция | Уравнение |
|---|---|
| Гидролиз воды | 2H2O → 2H+ + 2OH- |
| Окислительно-восстановительная реакция | 2H2O + 2e- → H2 + 2OH- |
| Фотосинтез | 6CO2 + 6H2O → C6H12O6 + 6O2 |
В заключение, H2O в химии представляет собой формулу для воды, которая является важным и уникальным веществом. Она обладает поларностью, способностью растворять другие вещества и участвовать в различных химических реакциях. Понимание свойств и реакций H2O имеет большое значение не только в химии, но и в биологии, экологии и других областях науки.
Описание
Вода является одним из наиболее известных и распространенных соединений. Она имеет множество уникальных свойств, которые делают ее необходимым и важным веществом для поддержания жизни на Земле. Вода является универсальным растворителем, реагентом во многих химических реакциях и жизненно важным компонентом для всех организмов.
Вода может быть вовлечена в различные химические реакции. Например, при нагревании воды до 100 °C она начинает кипеть и превращается в пар (H2O). Это происходит из-за разрушения ковалентных связей между атомами воды в процессе испарения. Пар обратно конденсируется в воду при охлаждении.
Одна из реакций, в которой участвует вода, это гидролиз. Гидролиз - это реакция, при которой вода разлагается на ионы H+ и OH-. Например, воду можно гидролизовать, добавив в нее малое количество кислоты или щелочи. В результате гидролиза образуются ионы, которые могут участвовать в других химических реакциях.
Другим примером реакции, в которой участвует вода, является нейтрализация. При нейтрализации кислота и щелочь реагируют в водной среде, образуя соль и воду. Например, реакция между соляной кислотой (HCl) и гидроксидом натрия (NaOH) приводит к образованию соли хлорида натрия (NaCl) и воды (H2O).
Формула 2H2O

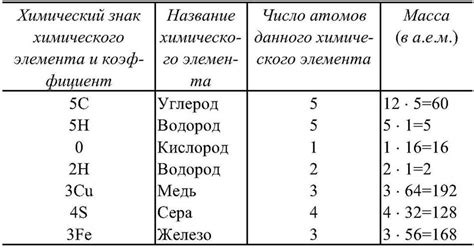
Формула 2H2O означает, что в реакции присутствуют две молекулы воды (H2O). Вода (H2O) состоит из двух атомов водорода (H) и одного атома кислорода (O). Поэтому формула 2H2O обозначает наличие четырех атомов водорода (2H) и двух атомов кислорода (O).
Реакция, в которой участвует 2H2O, включает в себя две молекулы воды и может протекать в различных химических процессах. Например:
- Электролиз воды: при применении электрического тока к 2H2O можно разложить молекулы воды на водород (H2) и кислород (O2), в результате чего получается 2 молекулы водорода и 1 молекула кислорода:
- 2H2O → 2H2 + O2
- 2H2 + O2 → 2H2O
Формула 2H2O является базовой для многих реакций, поскольку вода широко используется в химических процессах и имеет важное значение в жизни многих организмов, включая людей.
Примеры реакций с 2H2O
Примеры реакций с 2H2O включают:
| Реакция | Описание |
|---|---|
| 2H2O -> 2H2 + O2 | Деление воды на водород и кислород при помощи электролиза. |
| CaO + H2O -> Ca(OH)2 | Реакция нейтрализации между оксидом кальция (CaO) и водой (H2O), в результате которой образуется гидроксид кальция (Ca(OH)2). |
| 2H2O2 -> 2H2O + O2 | Распад перекиси водорода (H2O2) на воду (H2O) и кислород (O2). |
| H2 + Cl2 -> 2HCl | Реакция синтеза хлороводорода (HCl) из водорода (H2) и хлора (Cl2). |
| 2H2O + CO2 -> H2CO3 | Реакция обратимого образования угольной кислоты (H2CO3) из воды (H2O) и углекислого газа (CO2). |
Это лишь некоторые примеры реакций, в которых участвует 2H2O. Вода является универсальным растворителем и участвует во многих процессах в природе и в промышленности.
Важность 2H2O в химии
2H2O может быть продуктом или реагентом в различных химических реакциях. Например, в химической реакции горения, 2H2O образуется как продукт. Она также может быть использована в химических реакциях в качестве реагента, например, для гидратации алкенов или образования кислотных растворов.
Вода также является полезным растворителем для множества химических веществ, что делает ее важным компонентом в многих химических процессах. Благодаря своим уникальным свойствам, она способна растворять множество соединений и переносить их в реакции.
Кроме того, вода играет роль в химическом равновесии и общей кинетике химических реакций. Ее наличие или отсутствие может повлиять на скорость и направление реакции, а также на концентрацию реагентов и продуктов.
Таким образом, 2H2O имеет большое значение в химии, поскольку она является важным партнером во множестве химических реакций, влияет на физические свойства соединений и является неотъемлемой частью химических процессов.








