Характер высшего оксида - это химический термин, используемый для описания состояния оксида, когда между атомом металла и атомом кислорода существует сильная полярность связи. В характерном высшем оксиде атом кислорода претерпевает отрицательное ионное смещение, а атом металла приобретает положительный заряд.
Характерные высшие оксиды обладают различными свойствами и широко используются в различных областях науки и промышленности. Например, оксид алюминия (Al2O3) является одним из самых распространенных характерных высших оксидов и обладает высокой термической стабильностью, жаропрочностью и электроизоляционными свойствами. Это делает его идеальным материалом для использования в производстве электронных компонентов и антифрикционных покрытий.
Кроме того, другим примером характерного высшего оксида является оксид железа (Fe2O3), который широко применяется в производстве красок, стекла и керамики благодаря своей высокой красоте и прочности.
Значение характерного высшего оксида заключается в его способности к реакции с другими веществами и металлами, что используется в химической промышленности для получения различных продуктов. Однако, характерные высшие оксиды могут также быть вредными, так как они являются основными источниками загрязнения окружающей среды и вызывают проблемы с кислотными дождями и изменением климата.
Что такое характер высшего оксида
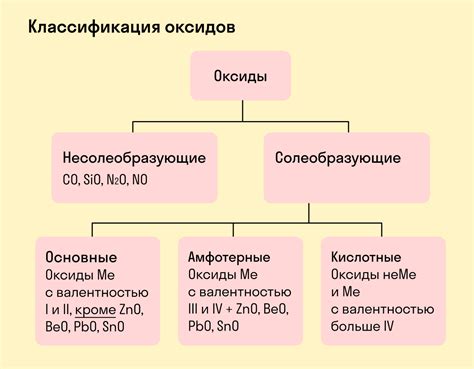
Высший оксид может иметь кислый, щелочной или амфотерный характер в зависимости от своих свойств.
Если при реакции с водой высший оксид образует кислоты, он называется кислотным высшим оксидом. Примером такого оксида является углекислый газ (CO2), который образует угольную кислоту (H2CO3) в реакции с водой.
Если же высший оксид образует щелочи при реакции с водой, он называется щелочным высшим оксидом. Примером такого оксида является гидроксид натрия (NaOH), который образует щелочное растворение с водой.
Наконец, если высший оксид образует как кислоты, так и щелочи при реакции с водой, он называется амфотерным высшим оксидом. Примером такого оксида является оксид алюминия (Al2O3), который может образовывать как кислотные, так и щелочные растворы в зависимости от условий.
Характер высшего оксида имеет важное значение для понимания его свойств и способности взаимодействовать с другими веществами. Он играет важную роль в химических реакциях и процессах, таких как диссоциация и нейтрализация.
Понятие характера высшего оксида
Такие оксиды взаимодействуют с водой, выделяя кислоты, и могут образовывать с ней кислотные растворы. Характер высшего оксида связан с его электрохимическими свойствами, а именно с тем, какие ионы оксида образуются в реакции с водой.
Примерами высших оксидов являются оксиды металлов, такие как оксид серы (SO3), оксид фосфора (P2O5) и оксид азота (NO2).
Значение характера высшего оксида заключается в его способности проводиться в реакции с водой и образовывать кислоты. Это свойство может быть использовано в различных химических процессах и промышленных производствах, где требуется получить кислотные растворы для дальнейшего использования.
Определение характера высшего оксида

Кислотные оксиды образуют кислоты при соединении с водой. Например, углекислый газ (CO2) реагирует с водой и образует угольную кислоту (H2CO3).
Основные оксиды образуют основания или гидроксиды при взаимодействии с водой. Например, оксид натрия (Na2O) реагирует с водой и образует гидроксид натрия (NaOH).
Амфотерные оксиды могут проявлять свойства как кислоты, так и основания при реакции с водой. Например, оксид алюминия (Al2O3) может образовывать ионы алюминия (Al3+) и гидроксидный ион (OH-).
Знание характера высшего оксида позволяет определить его реакционную способность и использование в различных химических процессах.
Примеры характера высшего оксида
Примеры характера высшего оксида можно найти во множестве химических соединений и природных минералов:
1. Двуокись углерода (CO2)
Характер высшего оксида в двуокиси углерода проявляется в ее свойстве окрашивать индикаторы, а также влиять на показатели кислотности среды. Это объясняется наличием кислорода в молекуле CO2.
2. Двуокись азота (NO2)
Характер высшего оксида в двуокиси азота заключается в ее высокой токсичности и воздействии на окружающую среду. NO2 является сильным окислителем и способен вызвать ожоги и раздражение при длительном воздействии.
3. Трехокись хрома (CrO3)
Характер высшего оксида в трехокиси хрома проявляется в ее кислотности и окрашивающих свойствах. CrO3 используется в производстве красок и пигментов благодаря своей способности окрашивать различные материалы.
Это лишь некоторые примеры характера высшего оксида, которые демонстрируют свойства, обусловленные присутствием кислорода в оксиде и его степенью окисления.
Значение характера высшего оксида
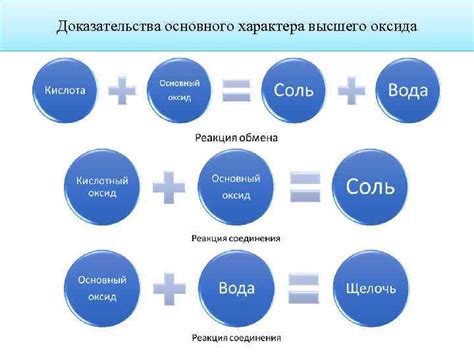
Характер высшего оксида представляет собой важную характеристику химического соединения. Он указывает на тип химической связи между атомами кислорода и других элементов, а также на окислительно-восстановительные свойства оксида.
Значение характера высшего оксида заключается в следующем:
| Характер высшего оксида | Значение | Примеры |
| Кислотный | Оксид обладает кислотными свойствами и реагирует с основаниями, образуя соль и воду. | SO3, CO2 |
| Основный | Оксид обладает основными свойствами и реагирует с кислотами, образуя соль и воду. | CaO, Na2O |
| Амфотерный | Оксид обладает как кислотными, так и основными свойствами и может реагировать как с кислотами, так и с основаниями. | Al2O3, ZnO |
| Нейтральный | Оксид не обладает ни кислотными, ни основными свойствами и не проявляет окислительно-восстановительных свойств. | CO, N2O |
Знание характера высшего оксида помогает предсказать его реакционные свойства и использование в различных процессах, таких как производство солей, водорода и других химических соединений.
Роль характера высшего оксида в химии
Характер высшего оксида характеризует его способность окислить или восстановить другие вещества. Он определяет, какой вид оксидов образуется при взаимодействии с определенным элементом или соединением, а также какие химические реакции могут происходить с участием данного оксида.
Примером является характер высшего оксида кислорода (О2), который обладает сильным окислительным свойством. Он способен окислять множество веществ, например, металлы, создавая при этом соответствующие оксиды. Кислородный характер оксида играет важную роль в многих процессах, включая горение, дыхание, окисление органических веществ и другие окислительные реакции.
Роль характера высшего оксида состоит не только в его влиянии на химические реакции, но и в его значимости для технологических процессов. Например, оксиды некоторых элементов используются как катализаторы в химической промышленности для ускорения реакций и повышения эффективности процессов. Знание характера высшего оксида позволяет оптимизировать условия проведения химической реакции и выбрать наиболее эффективные катализаторы.
Таким образом, характер высшего оксида играет важную роль в химической науке и промышленности. Он определяет свойства оксидов и их применение в различных областях, а также влияет на процессы окисления и восстановления в химических реакциях. Изучение характера высшего оксида является важной задачей химической науки и позволяет углубить понимание химических процессов и разработать новые технологии.








