Растворы являются основными объектами изучения химии и имеют огромное значение в различных отраслях науки и технологии. Реакции растворов являются процессами, при которых исходные растворы претерпевают изменения, сопровождающиеся образованием новых веществ. Они играют важную роль в различных химических реакциях, биохимических процессах, металлургии, фармакологии и других областях.
Основным принципом реакций растворов является взаимодействие ионов и молекул растворенных веществ между собой с образованием новых соединений. Эти реакции могут происходить как в присутствии воды, так и в других растворителях. Вода является одним из наиболее распространенных растворителей и обладает уникальными свойствами, способствующими проведению реакций растворов.
Важно отметить, что реакции растворов не всегда протекают полностью и могут быть обратимыми. Это значит, что новые соединения могут распадаться на исходные вещества. Такие реакции и их уравнения имеют большое значение в практическом применении и научных исследованиях.
Изучение реакций растворов позволяет расширить понимание принципов химических превращений, влияние факторов на процессы растворения и основных закономерностей образования новых соединений в растворах. Это помогает разрабатывать новые методы синтеза соединений, оптимизировать технологические процессы и повышать эффективность применения растворов в различных областях промышленности и науки.
Реакция растворов: основные механизмы и важность

Основными механизмами реакции растворов являются:
| 1. Реакция ионов | Растворы могут содержать ионы, которые могут реагировать друг с другом и образовывать новые соединения. Реакция ионов может происходить как в растворах электролитов, так и в некоторых органических растворах. |
| 2. Процессы диссоциации и ассоциации | В растворах могут происходить процессы диссоциации и ассоциации. Диссоциация - это процесс разделения молекулы на ионы при контакте с растворителем. Ассоциация - это процесс образования молекулы из ионов в растворе. |
| 3. Окислительно-восстановительные реакции | Растворы могут содержать вещества, которые могут переходить из одного окислительного состояния в другое. В результате таких реакций происходит обмен электронами между реагентами. |
Важность реакции растворов заключается в следующем:
- Позволяет получать новые вещества с заданными свойствами;
- Используется в синтезе химических соединений;
- Необходима для проведения аналитических исследований;
- Применяется в различных технологических процессах, например, в производстве лекарств, удобрений, красителей и других продуктов.
Таким образом, реакция растворов является важным принципом в области химии, который находит применение во многих областях науки и техники.
Взаимодействие растворов: понятие и примеры
Примеры взаимодействия растворов включают:
- Окислительно-восстановительные реакции. Например, при взаимодействии раствора хлорида натрия и раствора хлорида серебра происходит образование осадка серебра и выделение хлора.
- Кислотно-основные реакции. Например, при взаимодействии раствора соляной кислоты и раствора гидроксида натрия образуется раствор соли и вода.
- Процессы образования комплексных соединений. Например, при взаимодействии раствора CoCl2 и раствора NH3 образуется комплексное соединение [Co(NH3)6]Cl2.
- Процессы гидролиза. Например, при взаимодействии раствора соли аммония и раствора воды происходит расщепление ионов соли и образование гидроксида аммония.
- Процессы осаждения. Например, при взаимодействии раствора сернокислого натрия и раствора гидроксида кальция образуется осадок сернокислого кальция.
Понимание принципов и значимости взаимодействия растворов позволяет более глубоко изучать химические процессы, а также применять полученные знания на практике в различных областях, включая аналитическую химию, медицину и технологические процессы.
Реакция растворов и реакция веществ
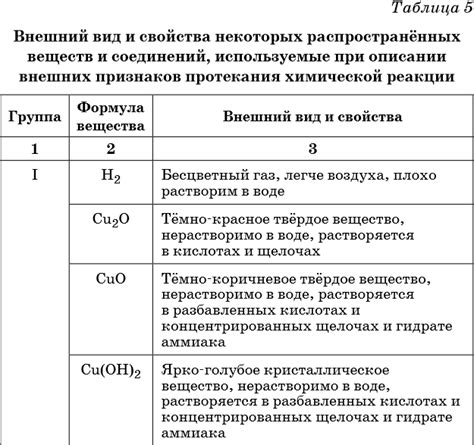
Реакция веществ - это процесс превращения одного вещества в другое с образованием новых химических связей. Реакции веществ могут происходить как в растворе, так и без него. Они могут быть вызваны различными факторами, такими как температура, давление, свет или электрическое поле.
Реакции растворов и реакции веществ играют важную роль в химии и имеют широкое применение в различных областях науки и технологии. Например, реакции растворов широко используются в аналитической химии для определения концентрации веществ в растворах. Реакции веществ могут быть использованы в синтезе новых веществ или для модификации свойств уже существующих материалов.
| Пример | Реакция растворов | Реакция веществ |
|---|---|---|
| 1 | Смешивание раствора серной кислоты с раствором натрия гидроксида, что приводит к образованию раствора соли и воды. | Нагревание углеводорода приводит к образованию диоксида углерода и воды. |
| 2 | Смешивание раствора хлорида натрия с раствором серебряного нитрата, что приводит к образованию осадка серебра. | Взаимодействие кислорода с железом приводит к образованию ржавчины. |
| 3 | Смешивание раствора азотной кислоты с раствором аммиака, что приводит к образованию аммония нитрата. | Окисление глюкозы приводит к образованию углекислого газа и воды. |
Реакции растворов и реакции веществ являются основой химических процессов и позволяют ученым изучать и изменять свойства веществ. Понимание принципов и механизмов этих реакций является важным шагом на пути к развитию новых материалов и технологий, которые могут иметь широкий применение в нашей жизни.
Химические и физические принципы реакции растворов
Химические принципы реакции растворов определяются характером взаимодействия различных веществ в растворе. Одним из основных факторов, влияющих на реакцию растворов, является реакционная способность веществ. Некоторые вещества обладают способностью взаимодействовать с другими веществами, образуя новые вещества, тогда как другие вещества могут быть пассивными и не проявлять реакционной активности.
Физические принципы реакции растворов связаны с изменениями физических свойств раствора при проведении химической реакции. Например, реакция растворов может приводить к изменению цвета раствора, изменению его температуры или изменению его состояния (например, переход от жидкого состояния к твердому или газообразному).
Химические и физические принципы реакции растворов взаимосвязаны и определяют итоговый результат реакции. Понимание этих принципов позволяет ученым и инженерам разрабатывать и улучшать процессы реакции растворов, а также находить новые способы применения растворов в различных отраслях промышленности.
Изучение химических и физических принципов реакции растворов имеет важное значение не только для профессионалов в области химии, но и для широкой публики. Знание этих принципов позволяет лучше понять мир вокруг нас и расширить свои знания в области науки и технологии.
Значение реакции растворов в природе
Реакция растворов играет важную роль в природе и влияет на многие процессы. Во-первых, реакция растворов влияет на химический состав воды в реках, озерах и морях. Природные водные растворы могут быть кислыми, щелочными или нейтральными, в зависимости от концентрации ионов водорода (pH).
Кислые растворы в природе, такие как дождевая вода, играют важную роль в процессах эрозии и растворения минералов. Они могут разрушать скалы и создавать впадины. Кроме того, кислые растворы способствуют образованию почвы, расщепляя минералы и освобождая питательные элементы для растений.
Щелочные растворы, такие как морская вода, также играют важную роль в природе. Они поддерживают жизнь многих организмов, включая морские водоросли и животных. Кроме того, щелочные растворы могут участвовать в процессах осадконакопления, таких как образование пустынных дюн.
Нейтральные растворы также находят свое применение в природе. Они могут служить водным средой для многих организмов и обеспечивать оптимальные условия для жизни. Нейтральные растворы также могут играть важную роль в процессах растворения и перемещения питательных веществ в почве.
Важно отметить, что реакция растворов в природе может изменяться под влиянием различных факторов, таких как загрязнение, изменение климата и геологические процессы. Это может иметь серьезные последствия для экосистем и биологического разнообразия.
| Тип раствора | pH | Примеры в природе |
|---|---|---|
| Кислый | меньше 7 | Дождевая вода, кислые озера |
| Щелочной | больше 7 | Морская вода, карстовые и пустынные озера |
| Нейтральный | 7 | Чистая вода, некоторые озера и реки |
Влияние температуры на реакцию растворов
Температура играет особую роль в химических реакциях, протекающих в растворах. Влияние температуры на реакцию растворов может быть существенным и приводить к изменению скорости и направления реакции.
При изм
Роль катализаторов в реакции растворов
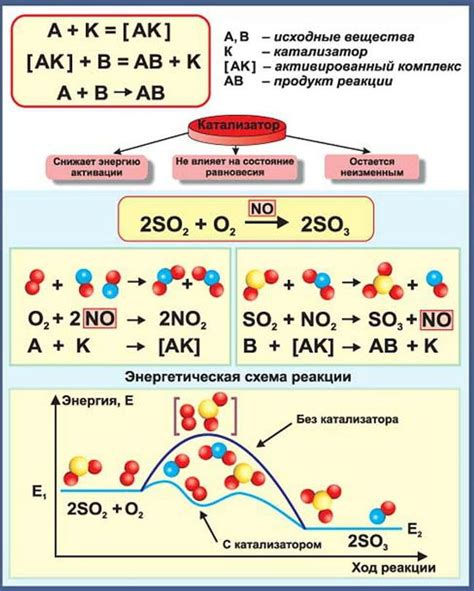
Одной из главных ролей катализаторов является обеспечение более быстрого и полного протекания реакции растворов. Катализаторы обладают специфичностью, то есть они совершают реакции только с определенными веществами и в определенных условиях. Они могут изменять скорость реакции, повышая или понижая ее, а также снижать необходимую температуру и давление для протекания реакции.
Катализаторы могут быть разделены на две основные категории: гетерогенные и гомогенные. Гетерогенные катализаторы находятся в другой фазе, чем реагирующие вещества, например, катализаторы могут быть в виде твердых частиц, на которых происходит реакция. Гомогенные катализаторы находятся в одной фазе с реагирующими веществами, например, катализаторы могут быть веществами в растворе.
Катализаторы широко используются в промышленности для повышения эффективности химических процессов. Они позволяют снизить затраты на энергию и сырье, увеличить выход продукта и улучшить качество реакционной смеси. Кроме того, катализаторы играют важную роль в окружающей среде, принимая участие в обработке отходов и очистке воздуха и воды.
| Преимущества катализаторов | Недостатки катализаторов |
|---|---|
| Ускорение реакции | Возможность отравления и деградации катализатора |
| Снижение энергозатрат | Высокие затраты на производство и обновление катализатора |
| Уменьшение вредных выделений | Сложность выбора и оптимизации катализатора |
В заключение, катализаторы играют важную роль в реакциях растворов, повышая их скорость и эффективность. Они являются необходимыми компонентами многих химических процессов и имеют широкое применение в промышленности и экологии. Однако, необходимо учитывать как их преимущества, так и недостатки при выборе и использовании катализаторов.
Измерение и учет реакции растворов
Для изучения и характеристики реакций растворов используют различные методы измерения и учета, которые позволяют определить и оценить процессы, происходящие в растворе.
Одним из основных методов является измерение реакции раствора с помощью индикаторов. Индикаторы – это вещества, которые меняют свой цвет или свойства при изменении pH-значения раствора.
Изменившийся цвет индикатора позволяет определить, насколько изменено pH-значение реакционной среды. Такие методы измерения используются, например, для контроля pH растворов в процессе химических реакций или для определения концентрации определенного иона в растворе.
Другой метод измерения реакции растворов - это использование спектров поглощения и испускания. Каждое вещество имеет определенный спектр поглощения и испускания света, который может использоваться для идентификации и количественного определения конкретных компонентов раствора. Например, спектроскопия позволяет измерить поглощение света раствором и определить его концентрацию или оценить степень реакции.
Также для измерения и учета реакции растворов используются различные методы анализа, такие как гравиметрический и титриметрический анализ. Гравиметрический анализ основан на определении массы полученного осадка или испарением раствора, что позволяет определить содержание конкретного компонента в растворе. Титриметрический анализ основан на измерении объема раствора стандартного реактивного вещества, реагирующего с компонентом в растворе, что позволяет определить его концентрацию.
Таким образом, измерение и учет реакции растворов являются важными этапами при изучении растворов и химических реакций. Они позволяют определить концентрацию, pH-значение, степень реакции и другие параметры, которые являются ключевыми для понимания и оценки процессов, происходящих в растворах.
Выводы и перспективы дальнейших исследований

Основные выводы, которые можно сделать на основе проведенных исследований:
- Реакция растворов играет важную роль в различных областях науки и технологии, таких как химия, медицина, окружающая среда и другие;
- Изучение реакции растворов позволяет определить условия ее протекания и оптимизировать эти условия для достижения желаемого результата;
- Свойства растворов могут значительно изменяться в зависимости от концентрации реагентов, температуры, pH и других факторов;
- Реакция растворов может регулироваться различными способами, такими как изменение концентрации реагентов, температуры, добавление катализаторов;
- Исследование реакции растворов имеет практическое значение для разработки новых материалов, лекарственных средств, методов анализа и других областей применения.
Дальнейшие исследования в этой области могут расширить наше понимание реакции растворов и привести к развитию новых методов и технологий. Более глубокое изучение механизмов реакции растворов может помочь улучшить существующие процессы и разработать новые, более эффективные решения.
В целом, исследование реакции растворов имеет большое значение для науки и промышленности, и может принести значительные практические преимущества. Развитие этой области исследований открывает широкие перспективы для применения усовершенствованных реакций растворов в различных областях жизни и деятельности человека.








