Взаимодействие молекул – это явление, которое играет ключевую роль во всех химических реакциях и процессах. Оно определяет, как одна молекула взаимодействует с другой и какие изменения происходят в результате этого взаимодействия. Взаимодействие молекул важно для понимания таких фундаментальных процессов, как образование и разрушение связей между атомами, передача энергии и информации.
Молекулы могут взаимодействовать различными способами. Одной из основных форм взаимодействия является химическая реакция, которая приводит к образованию новых веществ. В ходе химической реакции молекулы сталкиваются, меняют свою структуру и образуют новые связи, что приводит к изменению их свойств.
Взаимодействие молекул приводит к возникновению различных физических и химических феноменов, включая силы взаимодействия, изменение температуры и давления, образование растворов и многое другое.
Чтобы понять, как происходит взаимодействие молекул, необходимо учитывать их структуру и свойства. Молекулы могут притягиваться друг к другу или отталкиваться, в зависимости от химического состава и положения их атомов. Силы взаимодействия могут быть различными – ионными, ковалентными, ван-дер-ваальсовыми и другими.
Взаимодействие молекул: как это работает?
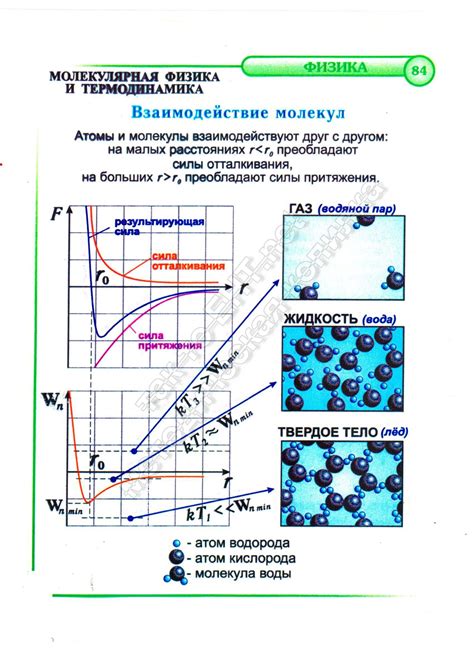
Основными видами взаимодействия молекул являются межмолекулярные силы и химические связи.
Межмолекулярные силы - это слабые силы притяжения между молекулами. Они объясняют, почему жидкости имеют поверхностное натяжение, а вещества могут переходить из одной фазы в другую. Межмолекулярными силами являются силы ван-дер-Ваальса, диполь-дипольное взаимодействие и силы ион-диполь.
Химические связи - это сильные силы притяжения между атомами, которые обеспечивают образование химических соединений. Они представляют собой обмен или перераспределение электронов между атомами. Химические связи делятся на ионные, ковалентные и металлические.
Взаимодействие молекул играет ключевую роль во многих жизненно важных процессах, таких как фотосинтез, дыхание, химические реакции и многое другое. Понимание механизмов взаимодействия молекул позволяет ученым разрабатывать новые материалы, лекарства и технологии, а также понимать и предсказывать различные физические и химические явления.
Основные понятия:
Основными понятиями, связанными с взаимодействием молекул, являются:
- Межмолекулярные силы: это силы, действующие между молекулами и определяющие их взаимодействие. Они могут быть притяжительными или отталкивающими и влиять на физические свойства вещества, такие как плотность, вязкость и т.д. Примерами межмолекулярных сил являются ван-дер-ваальсовы силы, водородные связи и ионные связи.
- Трехмерная структура молекулы: каждая молекула имеет свою уникальную трехмерную структуру, которая определяется расположением атомов и связей между ними. Эта структура может быть изменена при взаимодействии с другими молекулами.
- Межатомное взаимодействие: это взаимодействие между атомами внутри молекулы. Оно может быть сильным или слабым и зависит от электронной структуры атомов. Межатомное взаимодействие играет важную роль в образовании и стабильности молекул.
- Реакции между молекулами: это процессы, при которых молекулы перестраивают свою структуру, образуя новые связи и обменявшись атомами или группами атомов. Реакции между молекулами являются основой химических превращений и позволяют синтезировать новые вещества.
Понимание основных понятий взаимодействия молекул позволяет лучше понять многообразие химических и физических свойств веществ и применять эту информацию в различных научно-технических областях.
Химические связи:
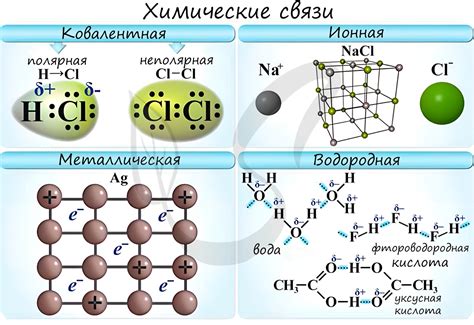
Существуют три основных типа химических связей:
| Ионная связь | происходит между положительно и отрицательно заряженными ионами. В этом типе связи один или несколько электронов переходят от одного атома к другому, создавая кулоновскую притягивающую силу. |
| Ковалентная связь | происходит, когда два атома делят пару электронов. Обычно образуется между неметаллами и может быть полярной или неполярной, в зависимости от разности электроотрицательности атомов. |
| Металлическая связь | является характерной для металлов. Она возникает из-за образования мобильной "облако электронов", которое связывает положительно заряженные ядра металлических атомов. |
Кроме основных типов химических связей, существуют и другие виды, такие как водородная связь и ван-дер-ваальсово взаимодействие, которые могут влиять на стабильность и свойства химических соединений.
Знание о химических связях помогает понять, как молекулы взаимодействуют друг с другом и как образуются различные химические соединения, что играет важную роль в химии и других науках.
Интермолекулярные силы:
Существует несколько типов интермолекулярных сил:
- Ван-дер-Ваальсовы силы. Эти силы возникают за счет недостаточной симметрии распределения электронов в молекуле и создают временные диполи. Они слабы и действуют преимущественно на более длинные расстояния.
- Диполь-дипольные силы. Эти силы возникают между молекулами, у которых есть постоянный дипольный момент. Они сильнее ван-дер-ваальсовых, но все же значительно слабее ковалентных или ионных связей.
- Водородные связи. Данный тип сил возникает между молекулами, включающими атомы водорода, связанные с электроотрицательными атомами, такими как кислород, азот и фтор. Водородные связи очень сильны и обладают большой энергией.
- Ионо-дипольные силы. Они возникают между молекулами и ионами и сильно влияют на свойства вещества. Они более сильны, чем диполь-дипольные силы и слабее ковалентных связей.
Все эти силы вместе определяют свойства вещества и влияют на его физическое и химическое поведение.
Типы взаимодействий:
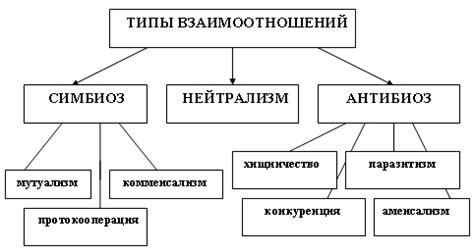
Взаимодействие молекул может происходить через различные типы сил притяжения и отталкивания. Ниже перечислены основные типы взаимодействий:
- Силы Ван-дер-Ваальса - это слабые притяжительные силы, возникающие между неполярными молекулами из-за временного неравномерного распределения электронов внутри молекулы.
- Электростатические силы - это притяжение или отталкивание зарядов между молекулами. Они играют ключевую роль в взаимодействии положительных и отрицательных ионов, а также в образовании водородных связей.
- Водородные связи - это сильные электростатические взаимодействия между молекулами, где водородный атом служит как донор или акцептор электронной пары. Водородные связи играют важную роль в структуре и свойствах многих веществ, включая воду и белки.
- Ионно-дипольное взаимодействие - это притяжение между ионами и полярными молекулами, где полярная молекула образует диполь, а ион обладает зарядом.
- Лонно-лигандное взаимодействие - это взаимодействие между ионами и комплексообразующими лигандами, где лиганд образует комплекс с ионом.
- Гидрофобное взаимодействие - это притяжение гидрофобных групп в молекулах, которые стараются избегать воды. Они связываются между собой, чтобы минимизировать контакт с водой.
Диссоциация и реакция:
Молекулы могут взаимодействовать друг с другом путем диссоциации и реакции. Диссоциация обычно происходит в результате сил притяжения или отталкивания между молекулами. В результате такого взаимодействия молекула распадается на ионы или другие молекулы.
Реакция представляет собой более сложный процесс, в который вовлечены две или более молекулы. В результате такой взаимодействия происходят химические изменения, и образуются новые вещества. Реакции могут происходить при наличии катализаторов или без них.
Диссоциация и реакция играют важную роль во многих химических процессах, таких как растворение веществ, нейтрализация кислот и щелочей, образование соединений и разложение веществ. Понимание этих процессов помогает лучше понять, как происходят химические реакции и взаимодействия между молекулами.
Физические и химические процессы:

Взаимодействие молекул может происходить через различные физические и химические процессы. Физические процессы основаны на изменении состояния или движения молекул без их заметного изменения. Они включают такие явления, как диффузия, конденсация, испарение и сублимация.
Конденсация происходит, когда газовые молекулы сближаются и образуют более крупные частицы жидкости. При испарении жидкостей, молекулы получают достаточно энергии, чтобы покинуть поверхность жидкости и стать газом. Диффузия представляет собой процесс перемещения молекул из области с более высокой концентрацией в область с более низкой концентрацией.
Химические процессы, в свою очередь, связаны с изменением состава и структуры молекул. Это включает реакции соединений, ассоциацию и диссоциацию молекул, а также образование новых соединений.
Реакции соединений – это процесс, при котором молекулы взаимодействуют друг с другом, чтобы создать новые соединения. Например, водород (H2) и кислород (O2) могут реагировать, образуя воду (H2O). Ассоциация молекул происходит, когда две или более молекулы объединяются для образования более крупного соединения, в то время как в диссоциации происходит распад молекулы на составные части.
| Процесс | Описание |
|---|---|
| Конденсация | Образование жидкости из газа |
| Испарение | Преобразование жидкости в газ |
| Диффузия | Распределение молекул от области с большей концентрацией к области с меньшей концентрацией |
| Реакции соединений | Молекулы взаимодействуют друг с другом, образуя новые соединения |
| Ассоциация молекул | Объединение двух или более молекул для создания более крупного соединения |
| Диссоциация | Распад молекулы на составные части |
Взаимодействие молекул через физические и химические процессы играет важную роль во многих аспектах нашей жизни, от обычных физических явлений, таких как кипение и горение, до сложных биологических процессов, таких как дыхание и пищеварение.








