Массовые доли элементов – это важная характеристика химических соединений, которая показывает, какое количество каждого элемента содержится в данном соединении. Расчет массовых долей необходим в химическом анализе, производстве и других областях химической науки. Правильное определение массовых долей элементов позволяет установить состав и свойства соединений и является основой для проведения различных химических реакций и процессов.
Методы расчета массовых долей элементов могут варьироваться в зависимости от конкретной задачи и свойств исследуемого соединения. Один из наиболее распространенных методов – метод мольного отношения. Он основан на отношении молейных количеств элементов в соединении. Другим способом является использование атомных и молекулярных масс элементов. Для этого необходимы данные о молекулярной формуле исследуемого соединения и атомных массах элементов. Также существуют методы, основанные на использовании расчетных формул и автоматических анализаторах, которые более точны и быстры в расчетах.
Расчет массовых долей элементов является важным шагом при проведении химических исследований и производственных процессов. Этот параметр позволяет определить количественное содержание каждого элемента в соединении, что имеет важное значение для оценки и контроля качества продукции. Знание основных понятий и методов расчета массовых долей элементов является необходимым для химиков и специалистов в области химической промышленности.
Определение массовых долей элементов

Одним из методов определения массовых долей элементов является химический анализ. При этом проводятся различные химические реакции и измерение массы реакционных продуктов. Из полученных данных можно вычислить массовые доли элементов.
Другим методом является спектральный анализ. Этот метод основан на измерении поглощения или испускания электромагнитного излучения различными элементами. По результатам такого анализа можно определить массовую долю элементов в смеси или веществе.
Ещё одним методом является гравиметрический анализ. Он основан на измерении массы отдельных компонентов смеси после проведения определенных химических реакций. Путем сопоставления полученных значений масс можно определить массовые доли элементов.
Определение массовых долей элементов является важной задачей в химии, так как по ним можно судить о составе и свойствах вещества или смеси. Точность и надежность определения массовых долей элеме
Значение массовых долей в химии
Массовая доля элемента в химическом соединении показывает, какой процент массы соединения приходится на данный элемент. Расчет массовых долей позволяет установить, какие элементы являются основными компонентами вещества и как они соотносятся друг с другом.
Массовые доли обычно выражаются в процентах или в виде десятичной дроби. Если массовая доля элемента равна 0,04 (или 4%), это означает, что вещество содержит 4 грамма этого элемента на 100 граммов общей массы.
Знание массовых долей в химии очень важно для проведения различных химических расчетов, так как позволяет определить не только состав вещества, но и пропорции компонентов. Это особенно важно при смешивании реагентов для получения продукта определенного состава или при вычислении массы вещества на основе его состава.
Расчет массовых долей осуществляется на основе данных о молекулярной массе элементов и соединений, а также на основе химической формулы вещества. Зная массовые доли, можно провести анализ и получить информацию о свойствах вещества и его возможных реакциях.
Понятие массы компонентов

Для расчета массовой доли элементов необходимо знать массу каждого компонента в смеси и общую массу всех компонентов. Общую массу можно определить путем сложения масс каждого компонента.
Массовая доля элемента X в смеси (Mx) вычисляется по формуле:
Мx = (масса элемента X / общая масса смеси) * 100%
Расчет массовых долей элементов в смеси позволяет определить количество каждого компонента и его вклад в общую составляющую. Это важно при изучении и анализе различных смесей, таких как сплавы, растворы или газовые смеси.
Методы определения массовых долей веществ
- Гравиметрический метод. В этом методе осуществляется определение массовых долей путем проведения взвешивания и измерения массы вещества, а затем его преобразования в процентное отношение к общей массе.
- Титриметрический метод. Этот метод основан на определении массовой доли вещества путем титрования пробы раствора с известным объемом стандартного раствора с известной концентрацией. При этом, известная концентрация раствора-титранта и его объем позволяют рассчитать массовую долю вещества в исследуемой пробе.
- Измерение плотности. В некоторых случаях, массовую долю вещества можно определить путем измерения плотности раствора с помощью специальных приборов. По данным о плотности и концентрации раствора можно рассчитать массовую долю вещества.
- Спектральный анализ. Этот метод основан на изучении спектров поглощения или испускания вещества. Измерение интенсивности и частоты излучения позволяет определить массовую долю вещества и провести его качественную и количественную характеристику.
Выбор метода для определения массовых долей веществ зависит от типа вещества, его физических и химических свойств, а также от доступных лабораторных средств и возможностей. Правильно выбранный метод обеспечивает точность и надежность результатов.
Метод гравиметрического анализа

Принципиально, метод гравиметрического анализа заключается в реакции между анализируемым веществом и реагентом, образующим весовые формы соединений. Затем производится фильтрация, осаждение, высушивание и измерение массы образовавшегося осадка. Рассчитывается массовая доля элемента по формуле, основанной на лавесовских принципах.
Этот метод обладает высокой точностью и применяется в различных областях, таких как анализ минеральных и органических веществ, пищевых продуктов, воды, почвы и металлургических материалов. Гравиметрический анализ также может использоваться для определения массовых долей различных элементов в смесях и растворах.
Важной характеристикой метода является его способность к эффективному разделению элементов и возможность детектирования и определения элементов с массовыми долями ниже 0,01%. Однако требовательность к длительности и сложности процесса гравиметрического анализа делает его менее привлекательным по сравнению с более современными методами, такими как спектрофотометрия и хроматография.
Метод объемного анализа
Для проведения объемного анализа необходимо использовать закон Авогадро, который гласит, что равные объемы газов при одинаковых условиях содержат одинаковое количество молекул. Исходя из этого закона, можно установить пропорции между объемами различных газов в химической реакции.
Для проведения объемного анализа необходимо знать стехиометрические соотношения химической реакции, то есть пропорции, в которых реагируют различные вещества. Пропорции между количествами веществ можно выразить в виде отношений объемов газов, используя коэффициенты перед формулами веществ в уравнении реакции.
Для расчета массовых долей элементов с помощью метода объемного анализа необходимо знать молярные массы элементов и веществ, участвующих в реакции. После определения объемов газов и установления пропорций между объемами, можно вычислить отношение масс веществ, используя молярные массы.
Метод объемного анализа позволяет определить массовые доли элементов только в газовых реакциях или в реакциях, которые сопровождаются образованием или потреблением газов. Этот метод является одним из наиболее точных и надежных при расчете массовых долей элементов в химических реакциях.
Метод спектрофотометрии
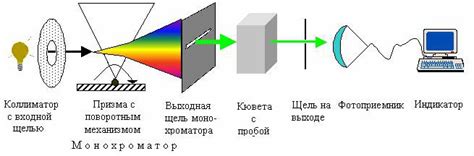
Принцип работы спектрофотометра основан на законе Бугера-Ламберта, согласно которому интенсивность света, поглощенного веществом, пропорциональна концентрации поглощающих веществ в растворе. Измерение поглощения происходит при помощи спектрофотометра – прибора, способного разлагать свет на компоненты разных длин волн и измерять их интенсивность.
Для проведения анализа методом спектрофотометрии необходимо подготовить образец вещества, который может быть в виде раствора или твердого образца. Затем вещество подвергается воздействию света определенной длины волны, и измеряется изменение интенсивности прошедшего через вещество света.
Измерение производится при помощи калибровочной кривой, которая строится путем измерения поглощения стандартных образцов с известной концентрацией. Затем, путем сравнения показателей поглощения и значениями на калибровочной кривой, определяются массовые доли элементов в исследуемом веществе.
| Длина волны, нм | Интенсивность поглощения |
|---|---|
| 350 | 0.75 |
| 400 | 0.60 |
| 450 | 0.45 |
| 500 | 0.30 |
| 550 | 0.15 |
В таблице представлен пример калибровочной кривой для определенного элемента. Используя эту кривую, можно определить концентрацию этого элемента в образце вещества путем измерения его поглощения при той же длине волны.
Таким образом, метод спектрофотометрии позволяет проводить точные и быстрые измерения поглощения вещества, что позволяет определить массовые доли элементов с высокой точностью.
Метод электрохимического анализа
Одним из основных методов электрохимического анализа является метод вольтамперометрии. Суть этого метода заключается в измерении зависимости между электрическим током, протекающим через электрод, и приложенным к нему потенциалом. По полученным данным можно определить массовые доли различных элементов в анализируемом веществе.
Еще одним методом электрохимического анализа является метод электродного потенциометрического титрования. В этом методе использование потенциометра позволяет измерять разность потенциалов на электроде, что позволяет определить концентрацию анализируемого вещества.
Метод электрохимического анализа широко применяется в различных областях, включая анализ воды, почв, пищевых продуктов и многих других.








