Галогенирование алканов - это химическая реакция, при которой в молекуле алкана атомы водорода заменяются на атомы галогена (хлора, брома, йода). Эта реакция является одной из важнейших реакций органической химии и широко применяется в промышленности для получения различных органических соединений.
Основными принципами галогенирования алканов являются стерические эффекты и электронные эффекты. Стерические эффекты определяют возможность замещения атомов водорода на атомы галогена в молекуле алкана, и они зависят от размера атомов галогена и замещаемого водорода. Электронные эффекты, такие как индуктивный эффект и электронное заполнение орбиталей, также играют важную роль в галогенировании алканов.
Галогенирование алканов имеет большое значение в органическом синтезе. Оно позволяет получать различные промежуточные соединения, которые могут быть использованы для получения более сложных органических соединений. Кроме того, галогенирование алканов может приводить к образованию соединений с новыми физическими и химическими свойствами, что позволяет использовать их в различных областях науки и технологии, включая фармацевтику, полимеры и материаловедение.
В заключение, галогенирование алканов является важным процессом, который позволяет получать разнообразные органические соединения и имеет широкое применение в промышленности и научных исследованиях. Понимание основных принципов этого процесса позволяет улучшить его эффективность и расширить его применение в различных отраслях химии.
Принципы галогенирования алканов

Основным принципом галогенирования алканов является замещение атомов водорода в молекуле алкана атомами галогена. Эта реакция может происходить под воздействием тепла или при участии катализаторов. Реакция галогенирования протекает по механизму радикального распада и механизму органической замещения, в зависимости от условий реакции.
Процесс галогенирования алканов в основном приводит к образованию смеси изомеров галогеналканов, так как замещение водорода может произойти на разных углеродных атомах молекулы алкана. Важным аспектом при галогенировании алканов является правильный выбор галогена и реакционных условий, так как они могут оказывать влияние на конечный продукт реакции.
Галогенирование алканов имеет большое значение в органическом синтезе и промышленности. Галогеналканы широко используются в производстве пластмасс, лекарственных препаратах, а также в качестве растворителей, антисептиков и огнезащитных веществ. Изучение принципов галогенирования алканов позволяет разработать эффективные методы синтеза галогеналканов и оптимизировать их производство.
Значение галогенирования алканов
Одним из основных применений галогенированных алканов является их использование в производстве пластмасс. Галогенирование позволяет улучшить физические и химические свойства материалов, таких как прочность, гибкость и огнестойкость.
Галогенированные алканы также широко применяются в фармацевтической и агрохимической промышленности. Они используются в производстве лекарственных препаратов, средств защиты растений и дезинфицирующих средств.
Кроме того, галогенирование алканов играет важную роль в области органической химии и синтеза новых соединений. Галогенирование может быть использовано в качестве стартового шага в синтезе различных органических соединений, таких как алкены, спирты, амины и карбонильные соединения.
В целом, галогенирование алканов имеет значительное практическое значение в различных областях, таких как промышленность, медицина и научные исследования. Он позволяет получать новые соединения с улучшенными свойствами и открывает возможность для развития новых технологий и материалов.
Химические реакции галогенирования алканов
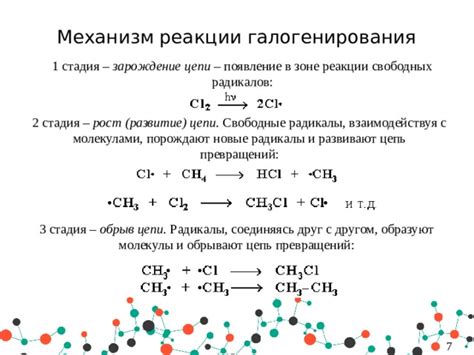
Галогенирование алканов с хлором и бромом происходит путем прямого замещения атомов водорода в молекуле алкана галогенными атомами. Это реакция субституции, в результате которой образуется халогеналкан. Реакционная способность галогенирования алканов возрастает с увеличением атома галогена в периоде и уменьшением атома галогена в группе Периодической системы.
Галогенирование алканов с хлором и бромом протекает по радикальному механизму. Сначала происходит инициация реакции, когда галоген (хлор или бром) разрывает свою связь и образует атомный радикал. Затем, радикал галогена атакует молекулу алкана и замещает один из атомов водорода, образуя галогеналкан и образовавшийся радикал алкана. Радикал алкана может продолжить реакцию, атакуя следующую молекулу галогена и так далее.
Реакция галогенирования с этилена (C2H4) также является значимой, поскольку в результате образуется полимер – полихлорэтилен. Полихлорэтилен широко используется в производстве пластиковых изделий, в том числе и упаковочных материалов.
Получение галогенированных алканов
Обычно для галогенирования алканов используются галогены (бром или хлор), а также катализаторы, которые помогают ускорить реакцию. В зависимости от условий реакции можно получить различные галогенированные алканы.
Наиболее распространенным методом получения галогенированных алканов является реакция замещения. В этой реакции атомы галогена замещают атомы водорода в молекуле алкана. Например, при реакции замещения хлорметана мы получаем хлорэтан:
CH3Cl + CH4 → CH3CH3 + HCl
Еще одним способом получения галогенированных алканов является реакция аддиции. При этом галогеноводороды (например, HBr или HCl) аддируются к двойной или тройной связи в молекуле алкена или алкина. Результатом реакции будет образование галогенированного алкана. Например:
CH2=CH2 + HCl → CH3CH2Cl
Также существуют и другие методы получения галогенированных алканов, такие как реакция галогенирования при высоких температурах и реакция радикального галогенирования. Все эти методы позволяют получить различные галогенированные алканы с разными свойствами и применениями.
Применение галогенированных алканов
Галогенированные алканы, полученные путем галогенирования алканов, имеют широкое применение в различных отраслях промышленности и научных исследованиях.
Одно из основных применений галогенированных алканов - это в качестве реагентов в органическом синтезе. Эти соединения могут служить исходными материалами для получения различных органических соединений, таких как спирты, эфиры, амины и др. Благодаря наличию галогенов в их структуре, галогенированные алканы могут участвовать в реакциях подстановки и электрофильного замещения, позволяя получать продукты с новыми свойствами и функциональными группами.
Также галогенированные алканы нашли применение в химической промышленности как растворители для органических и неорганических веществ. Они широко используются в процессах извлечения, очистки и разделения различных веществ. Галогенированные алканы также используются в производстве пластмасс, красителей, фармацевтических препаратов и других промышленных продуктов.
В медицине, галогенированные алканы, такие как хлороформ и фтораны, используются как анестетики для обезболивания при хирургических операциях. Они обладают сильным обезболивающим и седативным эффектом, благодаря чему могут быть применены в условиях общей анестезии.
Также галогенированные алканы могут быть использованы в качестве огнегасителей. Бромированные алканы, например, широко применяются во многих пожаро- и горючестойких материалах и покрытиях для предотвращения распространения огня.
Исключительная химическая активность и разнообразие свойств галогенированных алканов делают их полезными и востребованными соединениями в различных областях применения.








