Изомеры - это органические соединения, которые имеют одинаковый химический состав, но различаются по структуре и свойствам. Они обладают одинаковым числом атомов каждого элемента, но эти атомы могут быть распределены по-разному в пространстве. Изомеры могут различаться по молекулярной формуле, структурной формуле и линейности молекулы.
Изомеризм - это явление, при котором у различных соединений одного и того же элемента или группы элементов отличается не только химическая формула, но и строение молекулы. Изомеры могут образовываться как при замене атомов, так и при изменении их порядка в молекуле.
Изомеризм играет важную роль в химии, так как изомеры могут иметь различные физические и химические свойства. Например, изомеры могут отличаться по плотности, температуре плавления и кипения, растворимости, активности и стабильности. Также, изомеры могут иметь различные химические реакции и активность в биологических системах, что делает их интересными для изучения и применения в различных областях науки и промышленности.
Изомеризм может быть классифицирован на структурный и пространственный изомеризм. Структурный изомеризм связан с различным расположением атомов в молекуле, в то время как пространственный изомеризм связан с различным пространственным расположением атомов в пространстве. Примеры изомеров включают циклические и ациклические изомеры, а также изомеры с различными функциональными группами.
Что такое изомеры
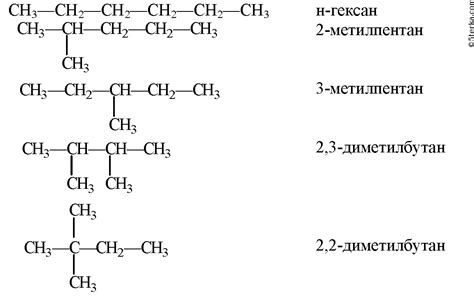
Изомерия возникает из-за различных способов соединения атомов в молекуле, изменения порядка их связей, перестановки групп или их пространственного расположения. Это может приводить к появлению новых химических свойств и возможностей.
Наиболее распространенные виды изомерии включают структурную изомерию, геометрическую изомерию и оптическую изомерию.
Структурная изомерия возникает, когда изомеры имеют различные связи атомов и/или разное расположение функциональных групп. Это может быть двойная или тройная связь, перестановка атомов или замена одного атома другим.
Геометрическая изомерия складывается из изомеров, у которых атомы связаны одним и тем же порядком связей, но имеют разное пространственное расположение. Это может быть вызвано наличием двойных связей, пространственными ориентациями групп или изгибами молекулы.
Оптическая изомерия возникает, когда молекулы имеют зеркальные изображения друг друга и не могут совместиться одинаковыми способами. Это в основном связано с асимметричными молекулами и приводит к возникновению двух оптических изомеров - Д- и Л-изомеров.
Изомерия играет важную роль в химии, поскольку позволяет различным соединениям с одинаковым составом проявлять различные свойства и функции. Изучение изомерии помогает понять молекулярную структуру и взаимодействие веществ.
Определение изомеризма в химии
В связи с этим, изомеры отличаются своими физическими и химическими свойствами. Это может проявляться в разных показателях, таких как плотность, кипячение, растворимость, активность и так далее. Изомеры могут обладать различной активностью и устойчивостью в разных условиях.
В химии выделяют различные типы изомеризма, включая структурный изомеризм, геометрический изомеризм, оптический изомеризм и так далее. Каждый тип изомеризма связан с конкретными изменениями в структуре молекулы и ее пространственном расположении.
Изомеризм играет важную роль в химических реакциях и биологических процессах. Изучение и понимание изомерии помогает ученым лучше понять свойства и поведение химических соединений, а также разрабатывать новые лекарственные препараты и материалы с нужными свойствами.
Различные виды изомерии
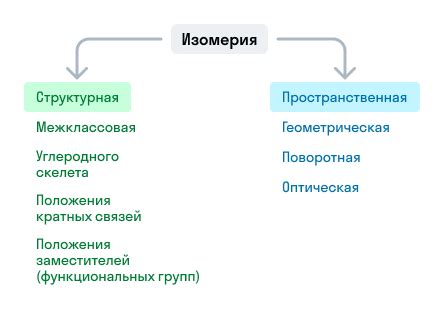
В химии существует несколько различных видов изомерии, которые по-разному описывают довольно сложные отношения между различными соединениями:
- Структурная (конституционная) изомерия: это вид изомерии, при котором молекулы имеют одинаковую молекулярную формулу, но отличаются внутренними связями и расположением атомов. Этот вид изомерии включает цепные (циклические), функциональные и геометрические изомеры.
- Стереоизомерия: этот вид изомерии характеризуется различной трехмерной структурой молекулы. Включает в себя такие виды как оптическая изомерия (энантиомерия), диастереоизомерия и конформационная изомерия.
- Таутомерия: это вид изомерии, при котором молекулы могут переходить друг в друга за счет изменения положения атомов в молекуле. Включает в себя гидратоформы и кето-энольные формы.
- Нуклеотидная изомерия: это вид изомерии, который возникает у нуклеотидов в ДНК и РНК. Включает в себя такие виды как граничная изомерия и конформационная изомерия.
Каждый из этих видов изомерии может играть важную роль в химической реакции и иметь различные физические и химические свойства.
Структурные изомеры
Например, пропан и изобутан являются структурными изомерами. Оба этих соединения имеют формулу C3H8, но атомы углерода расположены и связаны по-разному. В молекуле пропана все три атома углерода связаны в линейную цепочку, в то время как в молекуле изобутана центральный атом углерода связан с тремя другими атомами углерода, образуя ветвь.
Структурные изомеры обладают различными свойствами и могут иметь разные физические и химические свойства. Например, пропан является газом при комнатной температуре, а изобутан является газообразным веществом низкой температуры.
Изучение структурных изомеров позволяет лучше понять химическую реактивность и свойства органических соединений.
Функциональные изомеры

Функциональные изомеры имеют различные функциональные группы, но одинаковую молекулярную формулу. Это означает, что у них одинаковое количество атомов каждого элемента, но в различной конфигурации. Например, эфиры и алкены являются функциональными изомерами. Оба класса молекул имеют молекулярную формулу C4H8O.
Функциональные изомеры имеют различные физические и химические свойства. Они могут иметь различные точки плавления и кипения, а также различную реакционную способность. Например, алкены обладают двойной связью между атомами углерода, что делает их более реакционноспособными по сравнению с эфирами.
Функциональные изомеры являются важной концепцией в органической химии, поскольку они позволяют ученым объяснять различные химические свойства и реакционную способность различных классов органических соединений.
Конформационные изомеры
Конформационными изомерами называются изомеры, которые отличаются друг от друга только пространственным расположением атомов, сохраняя при этом последовательность связей.
Пространственное расположение атомов в молекуле определяется конформацией, которая характеризуется конкретным положением атомов в пространстве и углом поворота по химической связи. Конформационные изомеры могут существовать за счет вращения атомов вокруг одной или нескольких химических связей.
Конформационные изомеры обычно наблюдаются у молекул с одним или несколькими свободными вращательными связями, то есть у молекул, содержащих одинарные и двойные связи. Примером конформационных изомеров являются изомеры н-бутана, которые отличаются пространственным расположением метильных групп.
Конформационные изомеры могут существовать в разных конформациях, которые обусловлены энергетическими барьерами для вращения атомов. Некоторые конформации могут быть более стабильными, а другие – менее стабильными и иметь повышенную энергию. Конформационные изомеры могут переходить друг в друга путем конформационных изменений, которые происходят при изменении энергии системы.
Конформационные изомеры имеют важное значение в изучении структуры и свойств органических молекул. Измение конформации может влиять на физические и химические свойства молекулы, такие как плотность, температура плавления и кипения, активность их биологического действия и другие свойства.
Геометрические изомеры
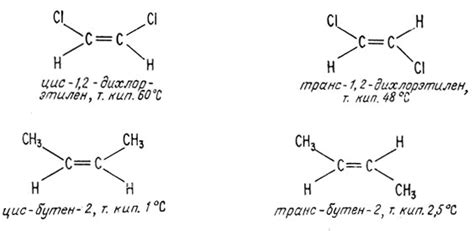
Главными видами геометрических изомеров являются изомеры З и Е. Изомеры З образуются, когда на одной стороне от двойной связи находятся атомы или группы атомов с большей массой, а на другой стороне - атомы или группы атомов с меньшей массой. Изомеры Е образуются, когда атомы или группы атомов с одинаковой массой находятся на одной стороне от двойной связи.
Основной пример геометрических изомеров - изомеры гексахлорциклогексана. В обоих случаях молекула содержит шесть атомов хлора и шесть атомов водорода, но они отличаются пространственным расположением. У изомера З все атомы хлора находятся на одной стороне молекулы, а у изомера Е атомы хлора чередуются.
Геометрические изомеры имеют различные физические и химические свойства. Например, они могут иметь различную активность в реакциях или различные точки плавления и кипения.
Примеры изомерии
1. Структурная изомерия
Структурная (конституционная) изомерия возникает при различном расположении атомов в молекуле. Например, этиловый спирт (CH3CH2OH) и метиловый эфир (CH3OCH3) – это структурные изомеры, так как у них разное расположение атомов кислорода.
2. Геометрическая изомерия
Геометрическая изомерия возникает у молекул, имеющих одинаковое расположение атомов, но отличающихся пространственной ориентацией. Например, цис-бутен и транс-бутен – это геометрические изомеры, так как у них разное пространственное расположение водородных атомов.
3. Оптическая изомерия
Оптическая изомерия связана с различными свойствами вещества в отношении поляризованного света. Например, L-альдопентоза и D-альдопентоза – это оптические изомеры, так как они отклоняют поляризованный свет в разные стороны.
Эти примеры иллюстрируют, что изомерия является обширным и разнообразным явлением, которое играет важную роль в органической химии.








