Вычисление массовых долей элементов в химии является важным шагом для понимания состава и свойств различных веществ. Массовая доля элемента вещества определяет, сколько граммов данного элемента находится в 100 граммах образца.
Для вычисления массовой доли элемента необходимо знать массу данного элемента в образце и общую массу образца. Массу элемента можно определить с помощью химического анализа, спектрального анализа или других методов. Общую массу образца можно измерить с помощью весов или других приборов.
Вычисление массовых долей элементов основано на принципе сохранения массы: сумма масс всех элементов в образце должна быть равна массе образца. Вычисленные массовые доли элементов часто используются для определения химической формулы вещества, для расчетов реакций или для анализа примесей.
Понятие и значение массовых долей в химии

Массовые доли имеют большое значение в химических расчетах и анализе веществ. Они позволяют определить состав и пропорции элементов в химическом соединении. Кроме того, массовые доли могут быть использованы для определения состава смесей и реакционных промежуточных продуктов, а также для проведения количественного анализа образцов.
Массовая доля элемента в веществе рассчитывается по формуле:
- Массовая доля элемента = (масса элемента в веществе / общая масса вещества) * 100%
Например, для воды (H2O) массовая доля водорода (H) составляет около 11%.
Знание массовых долей элементов позволяет установить соотношение атомов в химических соединениях и провести рассчеты по количественным химическим реакциям. Также массовые доли используются для стандартизации и обозначения концентрации растворов. Благодаря массовым долям, мы можем определить, какую часть массы в веществе составляет каждый элемент и как они взаимодействуют для образования новых соединений.
Что такое массовые доли элементов?
Массовые доли элементов в химии представляют собой величины, которые показывают, какую часть массы химического вещества составляет каждый его элемент. Вещество может состоять из нескольких элементов, и каждый элемент имеет свою массовую долю. Массовая доля элемента рассчитывается путем деления массы данного элемента на общую массу вещества и умножения результата на 100%.
Массовые доли элементов являются важной характеристикой вещества и используются для определения его состава и свойств. Они помогают химикам и исследователям понять, какие элементы присутствуют в веществе и в каком количестве. Массовые доли элементов можно использовать для расчета молекулярной массы вещества, проведения химических реакций и определения стехиометрии реакций.
Например, для воды (H2O) массовая доля водорода (H) равна 11,1%, а массовая доля кислорода (O) равна 88,9%. Это означает, что водород составляет около 11,1% массы воды, а кислород - около 88,9% массы.
Знание массовых долей элементов позволяет более точно описать вещество и проводить его химический анализ. Они также помогают понять, какие элементы могут проявлять определенные свойства вещества и как взаимодействуют друг с другом различные элементы при проведении химических реакций.
Как вычислить массовые доли элементов?
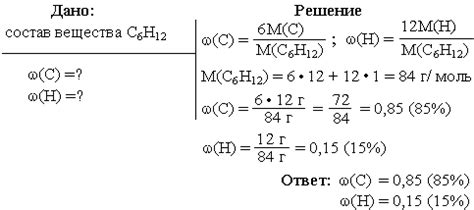
Для вычисления массовых долей элементов необходимо знать их массу и общую массу вещества. Массу элемента можно определить, используя различные методы анализа, такие как химический анализ или инструментальные методы анализа.
Вычисление массовых долей элементов может быть полезно в разных областях науки и промышленности. Например, в химии массовые доли элементов могут использоваться для определения состава химических соединений, расчета реакционной способности вещества и т.д.
Массовые доли элементов могут быть выражены в процентах или в долях единицы. Для выражения массовых долей элементов в процентах необходимо умножить полученную массовую долю на 100%.
Например, для вычисления массовой доли элемента X вещества Y можно воспользоваться следующей формулой:
Массовая доля элемента X = (масса элемента X / общая масса вещества Y) * 100%.
Таким образом, вычисление массовых долей элементов может быть осуществлено путем деления массы элемента на общую массу вещества и умножения результата на 100%.
Также следует помнить, что сумма массовых долей всех элементов вещества должна быть равна 100%, так как общая масса вещества представляет собой 100% его состава.
Вычисление массовых долей элементов позволяет получить информацию о составе вещества, его свойствах и возможных применениях, что делает этот процесс важным в химических исследованиях и технологиях.
Примеры расчетов массовых долей элементов
Ниже приведены несколько примеров расчетов массовых долей элементов для различных соединений:
Пример 1: Расчет массовой доли кислорода в воде.
Молекула воды (H2O) состоит из двух атомов водорода (масса атома H = 1) и одного атома кислорода (масса атома O = 16).
Масса молекулы воды: 2 * 1 + 16 = 18.
Массовая доля кислорода: (16 / 18) * 100% = 88,89%.
Массовая доля водорода: (2 / 18) * 100% = 11,11%.
Пример 2: Расчет массовой доли карбона в метане.
Молекула метана (CH4) состоит из одного атома углерода (масса атома C = 12) и четырех атомов водорода (масса атома H = 1).
Масса молекулы метана: 12 + (4 * 1) = 16.
Массовая доля карбона: (12 / 16) * 100% = 75%.
Массовая доля водорода: ((4 * 1) / 16) * 100% = 25%.
Пример 3: Расчет массовой доли азота в аммиаке.
Молекула аммиака (NH3) состоит из одного атома азота (масса атома N = 14) и трех атомов водорода (масса атома H = 1).
Масса молекулы аммиака: 14 + (3 * 1) = 17.
Массовая доля азота: (14 / 17) * 100% = 82,35%.
Массовая доля водорода: ((3 * 1) / 17) * 100% = 17,65%.
Эти примеры помогут вам лучше понять, как вычислять массовые доли элементов в различных химических соединениях.








