Возбужденный электрон – это электрон в атоме или молекуле, который находится в высокоэнергетическом состоянии, отличном от его основного состояния. Как только электрон получает энергию, он переходит в возбужденное состояние, оставаясь на нем какое-то время, прежде чем вернуться в свое основное состояние.
Возбуждение электрона происходит, когда атом или молекула поглощают энергию в виде света, тепла, электрического разряда или других источников. В результате возбуждения происходят изменения электронных уровней атома или молекулы, а также изменяются свойства электрона.
Возбужденные электроны имеют большую энергию и могут участвовать в различных химических реакциях, а также испускать или поглощать фотоны – кванты света. Изучение возбужденных электронов и их влияния на свойства вещества имеет большое значение для многих областей науки и техники.
Например, в физике и фотохимии возбужденные электроны играют важную роль при изучении светоизлучения, флуоресценции и люминесценции. В электронике и оптоэлектронике возбужденные электроны применяются для создания полупроводниковых приборов, таких как светодиоды и лазеры. В медицине возбужденные электроны используются для диагностики и лечения различных заболеваний, например, в радиотерапии.
Таким образом, понимание понятия и значения возбужденного электрона играет важную роль в различных научных и технических областях, а его изучение способствует развитию новых технологий и применений в будущем.
Электрон как элементарная частица
Электрон не имеет внутренней структуры и считается точечной частицей, то есть не имеет размеров. Он часто используется в качестве модели исследования свойств и состава вещества.
Электрон обладает свойством ферми-дираковской статистики - одинаковые электроны не могут находиться в одном и том же квантовом состоянии. Это явление называется принципом исключения Паули. Благодаря этому свойству, атомы образуют структуру и располагают электроны на различных энергетических уровнях и подуровнях.
Электрон также обладает импульсом и спином, и он взаимодействует с электромагнитным полем. Волновая природа электрона проявляется в его дуальной природе, которая объясняет его свойства как частицы (корпускулярные свойства) и как волны (волновые свойства).
Возбужденный электрон - это электрон, перешедший на более высокий энергетический уровень в атоме. Это возможно при поглощении энергии от внешнего источника, например, при воздействии света на атом. Когда возбужденные электроны возвращаются на более низкие уровни, они излучают свет, что часто приводит к ярким цветам вещества.
Возбуждение электрона: определение и процесс
Возбужденный электрон – электрон, который приобретает дополнительную энергию и переходит на высший энергетический уровень в атоме или молекуле.
В процессе возбуждения электрона, он поглощает энергию от внешних источников, например, от фотонов света. Фотон, воздействуя на атом или молекулу, передает свою энергию электрону, который переходит на более высокий энергетический уровень.
Возбуждение электрона может происходить в таких процессах, как фотоэффект, фотолюминесценция, фотохимические реакции и другие.
После возбуждения электрон остается на высших энергетических уровнях в течение короткого времени, после чего он возвращается на нижние уровни. При этом электрон избавляется от лишней энергии, излучая фотон соответствующей энергии. Это процесс называется дезактивацией.
Возбуждение электрона и его последующая дезактивация являются важными процессами в физике и химии, так как определяют свойства и реакционную способность атомов и молекул.
Энергетические уровни возбуждения
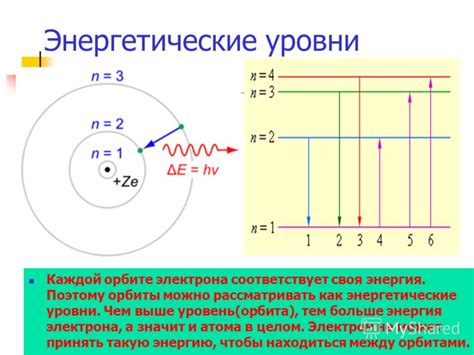
Атомы и молекулы имеют конкретные энергетические уровни, которые соответствуют различным энергетическим состояниям. На низшем энергетическом уровне находится основное состояние системы, в котором электроны находятся на своих основных орбиталях. При поглощении энергии электроны могут переходить на более высокие энергетические уровни, что приводит к возбуждению системы.
Энергетические уровни возбуждения атомов и молекул можно представить в виде энергетической диаграммы или энергетической таблицы. В таблице указывается энергия каждого уровня, а также определенные характеристики каждого состояния, например, магнитный момент или вращательная постоянная.
| Энергетический уровень | Энергия | Характеристики |
|---|---|---|
| Основное состояние | 0 | Нет возбуждения |
| Первый возбужденный состояние | 1 | Один электрон переходит на высшую орбиталь |
| Второй возбужденный состояние | 2 | Два электрона переходят на высшие орбитали |
Изменение энергии при переходе электронов на различные энергетические уровни возбуждения может приводить к различным физическим и химическим явлениям, таким как испускание света при рекомбинации электронов или изменение химической активности системы.
Понимание энергетических уровней возбуждения атомов и молекул имеет важное значение для различных областей науки и технологии, включая физику, химию, электронику и оптику.
Роль возбужденных электронов в химических реакциях
Возбужденные электроны играют важную роль в химических реакциях, они могут быть ключевым фактором в изменении химических связей и образовании новых соединений.
Когда электроны поглощают энергию, возбуждаются до более высоких энергетических уровней. Возбужденные электроны могут быть созданы различными способами, такими как поглощение фотонов света или передача энергии от других частиц.
Возбужденные электроны являются неустойчивыми и стремятся вернуться к своему исходному невозбужденному состоянию. Это можно достичь через эмиссию фотона света или передачу энергии другим частицам.
Когда возбужденные электроны обратно падают на более низкие энергетические уровни, они могут передать энергию другим атомам или молекулам. Этот процесс может создать различные изменения в структуре и свойствах взаимодействующих частиц.
Например, возбужденный электрон может передать энергию другой молекуле, вызывая ее разложение или изменение конформации. Возбужденные электроны также могут быть перенесены на реагирующие атомы, вызывая изменение их химической активности и способность принимать участие в химических реакциях.
Таким образом, возбужденные электроны являются важными участниками в химических реакциях, определяя подходящие условия для их протекания и влияя на механизмы реакций и образуемые продукты.








