Спирты являются одной из основных групп органических соединений, которые включают в себя различные классы алкоголей. В химии спирты определяются наличием гидроксильной группы (-OH) присоединенной к углеродному атому.
Примером группы спиртов являются первичные, вторичные и третичные спирты. Эти термины указывают на различное расположение гидроксильной группы относительно атомов углерода, которые она обслуживает.
Первичный спирт имеет гидроксильную группу, присоединенную к углеродному атому, который является прямо связанным с только одной другой углеродной группой. Вторичный спирт имеет гидроксильную группу, присоединенную к углеродному атому, который является связанным с двумя другими углеродными атомами. Третичный спирт имеет гидроксильную группу, присоединенную к углеродному атому, который, в свою очередь, является прямо связанным с тремя другими углеродными атомами.
Важно отметить, что присоединение гидроксильной группы к углеродному атому в спирте оказывает значительное влияние на его свойства и реакционную активность. Первичные, вторичные и третичные спирты обладают разной устойчивостью, а также образуют различные химические соединения при взаимодействии с другими веществами.
Определение первичных спиртов
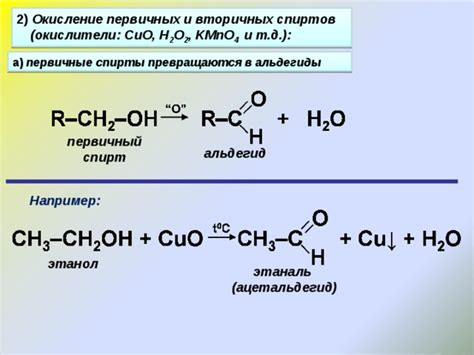
Первичные спирты обладают рядом химических и физических свойств:
| Свойство | Описание |
|---|---|
| Распространенность | Первичные спирты являются наиболее распространенным классом спиртов в природе, встречающимся в различных растениях, животных и микроорганизмах. |
| Органическое растворимость | Первичные спирты обычно хорошо растворяются в органических растворителях, таких как этанол, метанол и ацетон. |
| Воспламеняемость | Первичные спирты обладают высокими температурами вспышки и могут быть легко воспламенены открытым огнем или искрами. |
| Запах и вкус | Некоторые первичные спирты, такие как этанол (спиртовой спирт), обладают характерным запахом и вкусом. |
Признаки вторичных спиртов
Вторичные спирты отличаются от первичных и третичных спиртов своими особыми признаками. Ниже приведены основные признаки вторичных спиртов:
| Признаки | Описание |
|---|---|
| Группа функциональности | Вторичные спирты имеют группу гидроксильной функции (-OH) присоединенной к углеродному атому, который является вторичным (у него присоединены два других углеродных атома). |
| Общая формула | Общая формула вторичных спиртов: R2CHOH, где R - остаток органического соединения. Таким образом, вторичные спирты содержат два остатка углеродных атомов, присоединенных к центральному углероду, на котором находится гидроксильная группа. |
| Свойства | Вторичные спирты обычно имеют более высокую температуру кипения по сравнению с первичными спиртами. Они также обладают химическими свойствами, позволяющими проводить реакции окисления и превращения в альдегиды или кетоны. |
| Примеры | Примерами вторичных спиртов являются изопропиловый спирт (2-пропанол), бутиловый спирт (2-бутанол) и амиловый спирт (2-пентанол). |
Изучение признаков вторичных спиртов позволяет понять их структурные особенности и свойства, а также использовать их в различных областях науки и промышленности.
Особенности третичных спиртов

Важной особенностью третичных спиртов является их высокая степень окисления. Это связано с тем, что гидроксильная группа прикреплена к атому углерода, который уже образует три связи с другими атомами углерода. Из-за этого третичные спирты обладают высокой реакционной способностью и хорошими свойствами, что делает их полезными реагентами в синтезе органических соединений.
Химические свойства третичных спиртов определяют их способность к дегидратации и окислению. При дегидратации третичного спирта происходит удаление молекулы воды, что приводит к образованию двойной связи между атомами углерода. Окисление третичных спиртов может приводить к образованию кетонов или карбоновых кислот в зависимости от условий реакции.
Третичные спирты могут также подвержены реакции сильных окислителей, таких как хромовые кислоты, при которых образуются алдегиды или кетоны. Кроме того, третичные спирты обладают высокой температурой кипения и плотностью, что делает их более летучими и менее растворимыми в воде по сравнению с примарными и вторичными спиртами.
Основные свойства и применение различных типов спиртов
Первичные, вторичные и третичные спирты различаются по своей структуре и, соответственно, имеют разные свойства и применение.
- Первичные спирты: В первичных спиртах гидроксильная группа (-OH) связана непосредственно с одной углеводородной группой. Они обладают низкой кипящей точкой и хорошей растворимостью в воде. Первичные спирты часто используются в производстве этилового спирта, ацетона и других промышленных растворителей. Они нашли широкое применение в различных отраслях, включая химическую, фармацевтическую и пищевую промышленность.
- Вторичные спирты: Во вторичных спиртах гидроксильная группа (-OH) связана с двумя углеводородными группами. Они обладают высокой кипящей точкой и хорошей растворимостью в органических растворителях. Вторичные спирты широко используются в производстве растворителей, отжига и различных химических реакций.
- Третичные спирты: В третичных спиртах гидроксильная группа (-OH) связана с тремя углеводородными группами. Они обладают очень высокой кипящей точкой и малой растворимостью в воде. Третичные спирты находят применение в качестве растворителей, реагентов в органическом синтезе и в производстве лекарственных препаратов.
Каждый из типов спиртов имеет свои уникальные свойства, что делает их подходящими для различных приложений в разных областях работы с химическими веществами. Знание этих свойств и применение различных типов спиртов позволяет эффективно использовать их в различных химических и промышленных процессах.








