Отрицательная степень окисления – это определенное значение, показывающее количество электронов, которые атом вещества получает или делит с другим атомом во время химической реакции. Для атомов, имеющих электронную структуру элемента, отрицательная степень окисления указывает на то, что атом получает в электронную оболочку большее количество электронов, чем у элемента в свободном состоянии.
Окислители, вещества, способные окислять другие вещества, обладают положительной степенью окисления, в то время как вещества с отрицательной степенью окисления называют восстановителями. Отрицательное значение степени окисления свидетельствует о том, что атом имеет больше электронов, чем нормально для данного элемента. Это может быть связано с наличием одного или нескольких связей со степенью сцепления "covalent".
Примеры веществ с отрицательной степенью окисления включают анионы (отрицательно заряженные ионы), такие как хлорид и оксид, а также некоторые молекулы, такие как аммиак и гидриды. Важно отметить, что отрицательная степень окисления может изменяться в зависимости от конкретной химической реакции, так как электроны могут изменять свою принадлежность в разных условиях.
Что значит отрицательная степень окисления
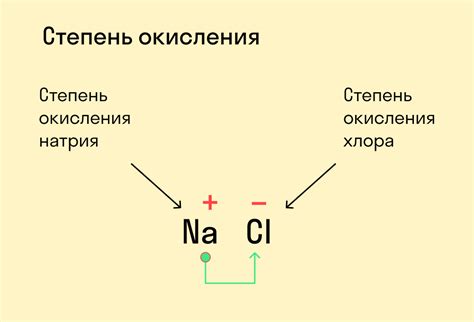
Вещества с отрицательной степенью окисления являются восстановителями, то есть способны отдавать электроны другим веществам при реакциях окисления. Они сами при этом окисляются. Часто такие вещества вступают в реакцию с веществами, имеющими положительную степень окисления, и передают электроны последним, причем количество переданных электронов равно модулю отрицательной степени окисления.
Примеры веществ с отрицательной степенью окисления включают гидриды металлов (например, NaH), металлы самого низкого электроотрицательности (например, самородное золото, Au), антиоксиданты (например, аскорбиновую кислоту, C6H8O6) и другие.
| Вещество | Отрицательная степень окисления |
|---|---|
| NaH | -1 |
| Au | 0 |
| C6H8O6 | -3 |
Определение и особенности
Вещества с отрицательной степенью окисления обычно являются окислителями, то есть способны передавать электроны другим атомам. Они проявляют активность в реакциях окисления и взаимодействии с веществами, имеющими положительную степень окисления.
Примерами веществ с отрицательной степенью окисления являются ионы водорода (H-) и молекулы некоторых соединений, таких как гидриды (например, натриевый гидрид - NaH).
Отрицательная степень окисления имеет важное значение в химии и позволяет определить активность и химические свойства веществ. Она также помогает в понимании механизмов реакций и переноса электронов в химических процессах.
Примеры веществ с отрицательной степенью окисления

В химии существуют вещества, у которых степень окисления атомов меньше нуля. Это связано с тем, что эти атомы получают электроны, тогда как обычно атомы отдают электроны и окисляются.
Некоторые примеры веществ с отрицательной степенью окисления:
- Водород (H-1)
- Литий (Li-1)
- Натрий (Na-1)
- Калий (K-1)
- Рубидий (Rb-1)
- Цезий (Cs-1)
- Ферроцианиды (например, Fe(CN)6-4)
Эти вещества имеют отрицательную степень окисления атомов, так как они получают электроны и становятся отрицательно заряженными.
Какие вещества имеют отрицательную степень окисления
Некоторые вещества, которые имеют отрицательную степень окисления, включают:
- Гидриды, например, натриевый гидрид (NaH) или натриевый боргидрид (NaBH4), где гидридный ион (H-) имеет отрицательную степень окисления.
- Металлы, которые находятся в области с отрицательной степенью окисления в периодической системе, например, железо (Fe), медь (Cu) и серебро (Ag).
- Полиатомные ионы, такие как сульфитный ион (SO32-), где центральный атом серы имеет отрицательную степень окисления.
Отрицательная степень окисления веществ является важным химическим свойством и играет роль во многих реакциях окисления-восстановления.
Бинарные соединения

Одно из важных свойств бинарных соединений - степень окисления элементов. Степень окисления - это числовое значение, которое показывает, сколько электронов получает или теряет атом элемента при образовании химического соединения. Обычно степень окисления указывается со знаком "+" или "-", где "+" обозначает потерю электронов, а "-" - получение.
В некоторых бинарных соединениях элемент может иметь отрицательную степень окисления. Например, в соединении фтора и кислорода - оксиде фтора (OF2), фтор имеет степень окисления "-1". Также, в сернистом ангидриде (SO2), сера имеет степень окисления "+4". Иногда бинарные соединения могут иметь элементы с разными степенями окисления, например, в перманганате калия (KMnO4), марганец имеет степень окисления "+7", а кислород - "-2".
Отрицательная степень окисления у элемента в бинарном соединении может указывать на его способность принимать электроны или быть окисленным другими элементами. Такие соединения часто обладают окислительными свойствами и могут быть использованы в химических реакциях.








