Окисление – это химический процесс, который происходит, когда вещество взаимодействует с кислородом. В результате такого взаимодействия происходит изменение состава вещества и его свойств. Окисление является одним из самых распространенных процессов в природе и играет важную роль в жизни многих организмов.
В химии окисление определяется как потеря электронов веществом. В процессе окисления атомы вещества увеличивают свой окислительный номер, а значит, увеличивают свою положительную зарядность. Это происходит за счет передачи электронов с одного атома на другой. В получившемся веществе, в результате окисления, содержится более высокоокисленное вещество и меньше электронов, чем в исходном составе.
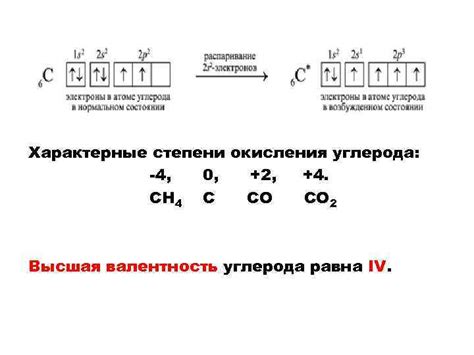
Важно отметить, что окисление и взаимодействие с кислородом не всегда сопровождается огнем и выделением тепла. Окисление может происходить и в холодных условиях.:
Окисление является важной частью многих процессов, происходящих в нашей жизни. Например, в дыхании окисление позволяет организму получить энергию из пищи. Окисление также играет ключевую роль в горении, ферментативных процессах, образовании ржавчины и других химических реакциях. Также следует отметить, что окисление может быть как желательным, так и нежелательным процессом, в зависимости от контекста и условий, в которых оно происходит.
Что такое окисление веществ
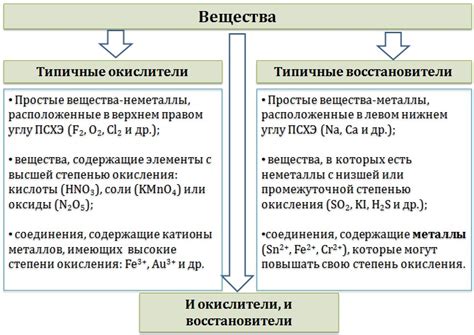
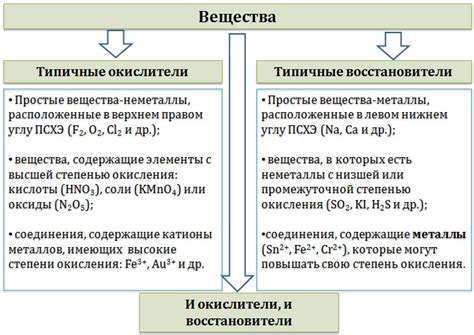
Во время окисления вещества подвергаются изменению своего окислительного состояния. Окисляющее вещество при этом получает электроны, а окисляемое вещество отдает электроны. Электроны передаются от одного атома к другому, что приводит к изменению их зарядов и образованию ионов.
Окисление является важным процессом во всех живых организмах, так как многие метаболические реакции, включая дыхание, зависят от этого процесса. В химической промышленности окисление используется для получения различных продуктов, в том числе кислот, альдегидов, кетонов и др.
Как происходит окисление веществ
Окисление и восстановление веществ могут происходить одновременно, они являются взаимосвязанными реакциями. В окислительно-восстановительных реакциях происходят переходы электронов от одних атомов к другим. В процессе окисления вещества на них воздействуют агенты окисления, которые способны принять электроны, а в процессе восстановления – агенты восстановления, которые способны отдать электроны.
Процесс окисления часто сопровождается появлением окисленных продуктов, а процесс восстановления – восстановленными продуктами. Эти продукты могут иметь различные свойства и применения. Окисление и восстановление широко используются во многих сферах, таких как химическая промышленность, медицина, пищевая промышленность и др.
Окисление веществ может происходить под воздействием тепла, света, катализаторов или других окислительных сред. Процесс окисления может быть быстрым или медленным в зависимости от условий. Некоторые окислительные реакции могут протекать самопроизвольно, а некоторые требуют энергии для инициирования.
Окисление веществ имеет важное значение в биологических системах. Дыхание, горение, окисление пищи – все эти процессы основаны на окислительно-восстановительных реакциях. Процесс окисления веществ играет важную роль в обмене веществ и энергии в организме.
Реакция окисления и воздействие кислорода

Кислород является одним из наиболее активных элементов, поэтому его воздействие может быть разнообразным и значительно влиять на окружающие объекты и процессы. К примеру, окисление железа приводит к образованию ржавчины, а окисление органических веществ может вызывать горение.
Окисление является одним из основных процессов в природе. Это, например, происходит при сжигании топлива в автомобиле или при дыхании организмов. Каждый раз, когда выдыхаем воздух, в нем содержится большое количество углекислого газа - продукта окисления.
В качестве окислителей в реакции окисления могут выступать не только кислород, но и другие вещества, например, пероксиды, азотные и хлорные соединения. В зависимости от условий, окисление может протекать существенно отличаться: с выделением тепла или его поглощением, медленно или очень быстро, с образованием газов или без.
Окисление веществ является важной частью многих процессов в технологии и промышленности. Например, окисление используется в процессе получения энергии из горючих ископаемых, а также в производстве различных химических веществ и материалов, таких как пластмассы, лекарственные препараты и многое другое.
Окисление и его влияние на свойства веществ
Окисление может происходить как на виду, например, когда металл теряет блеск и покрывается ржавчиной, так и невидимо, например, когда жирные кислоты окисляются в клетках организма, что может привести к развитию различных заболеваний.
Окисение может также влиять на хранение и стабильность веществ. Для некоторых продуктов окисление может быть полезным процессом, например, вино приобретает свой характерный вкус и аромат благодаря окислению в процессе ферментации. Однако для других веществ окисление нежелательно, поскольку может привести к потере питательных веществ, изменению текстуры или даже ухудшению качества товара.
Для защиты веществ от окисления можно использовать различные методы, например, хранение в вакууме, добавление антиоксидантов или использование специальных упаковок.
В целом, окисление является важным физико-химическим процессом, который играет значительную роль во многих областях, включая химию, биологию, пищевую промышленность и медицину.
Характерные признаки окисления
| Признак окисления | Пример |
|---|---|
| Потеря электронов | Атом железа Fe переходит в ион Fe2+ |
| Появление положительного заряда | Молекула кислорода O2 разрывается на ионы O+ |
| Увеличение окислительного числа | Атом меди Cu (окислительное число равно 0) окисляется до иона Cu2+ (окислительное число равно +2) |
Характерные признаки окисления могут помочь в определении, происходит ли реакция окисления. Они позволяют увидеть изменения в окислительном состоянии элементов и отследить передачу электронов в химической системе.
Процессы окисления в живых организмах
Главной молекулой, ответственной за окисление в клетках, является аденозинтрифосфат (АТФ) – универсальный носитель энергии. АТФ поступает в клетку извне или синтезируется внутри нее путем окисления органических веществ. Процесс синтеза АТФ называется фосфорилированием, и он является результатом серии окислительных реакций, происходящих внутри митохондрий.
Основные пути синтеза АТФ в клетке – это окислительное фосфорилирование и субстратное фосфорилирование. При окислительном фосфорилировании происходит превращение энергии, полученной от окисления органических веществ, в энергию связи фосфатов в молекуле АТФ. А при субстратном фосфорилировании фосфат присоединяется к АДФ непосредственно из органических молекул, не связанных с дыхательной цепью.
Окисление в клетках сопровождается образованием реактивных кислородных видов (РКВ), таких как супероксиды, перекись водорода и гидроксильные радикалы. Они являются продуктами неполного окисления органических веществ, а также образуются в результате воздействия внешних факторов, таких как ультрафиолетовое излучение и загрязнение окружающей среды.
РКВ имеют высокую активность и способны атаковать биологические молекулы, такие как белки, липиды и ДНК. Это может привести к повреждению клеток и возникновению различных патологических состояний, включая рак, старение и сердечно-сосудистые заболевания.
В организме есть системы, которые защищают клетки от действия РКВ. Одной из таких систем являются антиоксиданты. Они способны блокировать активность РКВ и предотвращать их вредное влияние на клетки. К таким антиоксидантам относятся витамин С, витамин Е, бета-каротин и другие.
Таким образом, процессы окисления и антиоксидантная защита играют важную роль в функционировании живых организмов. Понимание этих процессов необходимо для изучения различных биологических процессов, а также для разработки методов профилактики и лечения различных заболеваний.
Примеры окисления веществ в природе
1. Ржавчина на металлических предметах: Когда металлическая поверхность контактирует с влажным воздухом, образуется окисленный слой, известный как ржавчина. Это происходит из-за окисления железа в металле, которое приводит к образованию железного оксида.
2. Изменение окраски фруктов и овощей: Многие фрукты и овощи имеют яркую окраску благодаря наличию различных пигментов. Однако при воздействии кислорода из воздуха эти пигменты окисляются, что приводит к изменению окраски. Например, когда яблоки нарезаны и оставлены на воздухе, их мякоть становится коричневой.
3. Горение древесины: При сжигании древесины происходит окисление углерода в составе древесины. В результате этого процесса выделяется тепло и образуется углекислый газ.
4. Коричневение бананов: Когда бананы начинают коричневеть, это свидетельствует о процессе окисления. Фрукты содержат ферменты, которые при окислении приводят к разложению пигментов и изменению окраски.
5. Появление ржавчины на автомобилях: Металлические части автомобилей, такие как кузов и детали двигателя, подвержены воздействию окружающей среды. Когда металл контактирует с влагой, воздухом и солями, происходит окисление, в результате которого образуется коррозия и ржавчина.
Эти примеры показывают, как окисление веществ является неотъемлемой частью многих естественных процессов и имеет важное значение в природе.
Влияние окисления на окружающую среду
Окисление веществ особенно активно происходит при взаимодействии с кислородом воздуха. Это приводит к образованию различных оксидов, которые распространяются в атмосфере и могут являться причиной загрязнения воздуха.
Оксиды серы и азота, образующиеся при сгорании топлива в автомобильных двигателях и электростанциях, вносят значительный вклад в загрязнение атмосферы. Они являются источниками кислотных осадков и смога, что приводит к снижению качества атмосферного воздуха и негативно отражается на здоровье людей и экосистемах.
| Окислитель | Загрязняющие вещества |
|---|---|
| Кислород | Оксиды азота, оксиды серы, угарный газ |
| Хлор | Хлориды, хлораты, хлоргидриды |
| Бром | Бромиды, броматы |
Окисление веществ также может приводить к разрушению материалов и сооружений. Например, металлические конструкции могут подвергаться коррозии при контакте с кислородом и оксидами металлов.
В целом, влияние окисления на окружающую среду является серьезной проблемой, требующей постоянного внимания и принятия мер для минимизации его негативных последствий. Это включает разработку и применение новых технологий для очистки и предотвращения загрязнений, контроль выбросов вредных веществ, и повышение осведомленности общественности о важности сохранения окружающей среды.
Защита от окисления веществ

Окисление веществ может иметь разрушительное влияние на многие процессы в организме. Однако существует ряд механизмов, которые помогают защититься от негативных последствий окисления.
| Механизм защиты | Описание |
|---|---|
| Антиоксиданты | Антиоксиданты оказывают защитное действие, препятствуя окислительному стрессу. Они могут прямо или косвенно нейтрализовывать свободные радикалы, которые отвечают за окисление веществ. Антиоксиданты могут быть природными (витамин С и Е, бета-каротин) и синтетическими (бутилгидроксианизол, бутилгидрокситолуол). |
| Энзимы | Некоторые энзимы, такие как супероксиддисмутаза, пероксидазы и каталаза, способны эффективно обезвреживать свободные радикалы. Они катализируют реакции разложения оксидантов и предотвращают их вредное воздействие. |
| Металлосвязывающие белки | Металлосвязывающие белки, такие как трансферрин и ферритин, помогают снизить уровень свободных металлов в организме. Это важно, так как свободные металлы могут ускорить окисление веществ. |
Все эти механизмы взаимодействуют, обеспечивая баланс между образованием свободных радикалов и их устранением. Правильное питание, богатое антиоксидантами, а также здоровый образ жизни способствуют поддержанию эффективной защиты от окисления веществ.
Значение и применение окисления в различных отраслях
В промышленности окисление используется для получения множества продуктов. Например, в химической промышленности окисление позволяет получать различные кислоты и щелочи. Окисление также применяется в процессе синтеза органических соединений.
В производстве металлов окисление используется для получения металлических оксидов, которые после обработки превращаются в металлы. Благодаря окислительно-восстановительным реакциям многие металлы могут быть получены в чистом виде из своих руд.
В пищевой промышленности окисление играет важную роль в процессе приготовления пищи. Например, окисление жиров приводит к выделению аромата и создает своеобразный вкус. Кроме того, окисление может использоваться для увеличения срока годности продуктов путем уничтожения микроорганизмов.
В медицине окисление играет важную роль. Например, окисление используется в процессе дыхания, когда организм получает энергию из пищи. Окисление также используется в процессе борьбы с инфекцией, когда окислительные механизмы организма уничтожают вредоносные микроорганизмы.
Окисление имеет значение не только в промышленности, пищевой промышленности и медицине, но и во многих других отраслях. Например, в электрохимии окисление применяется для получения электрической энергии. В окружающей среде окисление играет роль в процессе образования ржавчины на металлических поверхностях.
Таким образом, окисление имеет большое значение и находит широкое применение в различных отраслях. Оно помогает получать продукты, улучшает качество пищи, обеспечивает жизненно важные процессы в организме и создает электрическую энергию. Это лишь некоторые примеры, демонстрирующие важность окисления в современном мире.








