НХ3 – это химическая формула аммиака, который является одним из основных веществ в химии. Аммиак представляет собой безцветный газ с резким и характерным запахом, который широко используется в различных отраслях и у обычных потребителей.
Основные свойства аммиака делают его уникальным веществом. Аммиак обладает высокими растворимостью и щелочной реакцией, что делает его полезным компонентом в производстве удобрений, химической промышленности и холодильной технике. Благодаря своей высокой растворимости, аммиак используется в медицине в качестве промывного и дезинфицирующего средства.
Аммиак также является важным сырьем для получения других химических соединений, таких как нитрат аммония, аммиачная селитра и многие другие. Благодаря своей щелочной реакции, аммиак используется в качестве компонента для очистки воды и сточных вод, а также в химическом анализе.
В заключение, аммиак (NH3) – это важное вещество в химии, обладающее множеством полезных свойств и широким спектром применения. Он используется в различных отраслях промышленности, медицине, сельском хозяйстве и других областях. Аммиак применяется в производстве удобрений, очистке воды, получении других химических соединений и многих других процессах. Его свойства и определение делают его незаменимым ингредиентом для множества промышленных и бытовых задач.
Аммиак: что значит NH3 в химии?

Аммиак имеет следующие свойства:
- Аммиак является газом без цвета и запаха.
- Он обладает высокой растворимостью в воде и гидратируется, образуя аммиачную жидкость.
- Аммиак является амфотерным веществом, способным реагировать как с кислотами, так и с основаниями.
- Он обладает щелочными свойствами и может реагировать с кислотами, образуя соли.
- Аммиак является отличным растворителем для многих веществ, в том числе для неорганических и органических соединений.
Аммиак используется во многих отраслях промышленности:
- В производстве удобрений: аммиак используется для производства аммиачной селитры, аммиачной селитровой селитры и других удобрений.
- В производстве пластмасс: аммиак используется в процессе синтеза мономеров для производства полиуретанов, полиамидов и других пластмасс.
- В производстве химических продуктов: аммиак используется в качестве сырья для производства различных химических соединений, например, нитратов, карбамидов, азотных кислот и др.
- В производстве чистки и отбеливания: аммиак используется в качестве компонента в процессе чистки и отбеливания текстиля и других материалов.
- В производстве пищевых продуктов: аммиак используется в некоторых процессах пищевой промышленности, например, для регулирования pH и как антиоксидант.
Определение аммиака и его формула NH3
Формула NH3 означает, что в молекуле аммиака находится один атом азота и три атома водорода. Молекулярный вес аммиака равен 17 единицам.
Аммиак широко используется в промышленности. Он применяется в качестве удобрения для улучшения почвы и роста растений. Он также используется в производстве химических веществ, таких как удобрения, пластмассы, красители и взрывчатые вещества.
Кроме того, аммиак используется в бытовых условиях в качестве чистящего средства. Он может быть добавлен к стеклянным или металлическим поверхностям для удаления пятен и загрязнений.
Из-за своей высокой растворимости в воде, аммиак может образовывать щелочные растворы. Он может быть использован для регулирования pH-уровня в водных системах или в лабораториях в качестве растворителя для различных химических реакций.
Химические свойства аммиака

Одной из основных химических свойств аммиака является его способность к образованию аммонийных солей. Аммиак реагирует с кислотами, образуя соли аммония. Например, аммиак может реагировать с соляной кислотой (HCl) и образовывать хлорид аммония (NH4Cl). Это свойство аммиака широко используется в производстве удобрений, так как аммонийные соли являются важными питательными веществами для растений.
Еще одним химическим свойством аммиака является его амфотерность. Аммиак может действовать как основание, принимая протон и образуя ион аммония (NH4+), а также может действовать как кислота, отдавая протон и образуя ион амида (NH2-). Это свойство аммиака позволяет ему реагировать с различными кислотами и основаниями, образуя разнообразные соединения.
Кроме того, аммиак обладает высокой растворимостью в воде. При контакте с водой аммиак образуетщ щелочную среду, образуя гидроксид аммония (NH4OH). Это свойство аммиака позволяет его использовать в качестве аммиачной щелочи в различных процессах, например, в качестве очистителя или в производстве лекарственных средств.
В целом, химические свойства аммиака делают его универсальным соединением с множеством применений в различных отраслях промышленности и науки.
Физические свойства аммиака
Температура кипения аммиака составляет -33,34°C при атмосферном давлении, что делает его одним из самых легких среди газов. При низких температурах (-77,7°C) аммиак может образовать замерзающую смесь с водой.
Аммиак является амфотерным веществом, что означает его способность реагировать как с кислотами, так и с щелочами. В воде он образует слабое основание – ион аммония (NH4+), который обладает положительным зарядом. Однако аммиак также может проявлять свойства кислоты и образовывать серные кислоты типа сульфата аммония (NH4)2SO4, облегчая взаимодействие с щелочами.
Аммиак обладает высокой растворимостью в воде. При комнатной температуре и давлении его максимальная растворимость составляет около 700 г/л. Растворы аммиака обладают щелочными свойствами и прекрасно реагируют с кислотами. Они находят широкое применение в различных областях, включая производство химических удобрений, очистку воды и производство пищевых продуктов.
Применение аммиака в промышленности
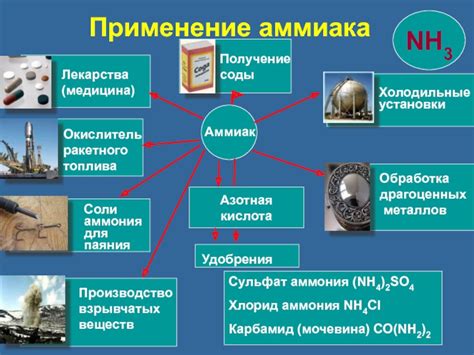
Аммиак (NH3) широко применяется в промышленности благодаря своим уникальным свойствам. Ниже приведены некоторые из основных областей его использования:
- Производство удобрений: аммиак является основным сырьем для производства азотных удобрений, таких как аммиачная селитра, карбамид и аммиачные фосфатные удобрения. Аммиак содержит азот, который является необходимым питательным элементом для растений.
- Химическая промышленность: аммиак используется в химической промышленности для производства различных химических соединений, включая нитраты, аммиачные соли, анилин и многое другое. Он также используется в процессах синтеза и окисления органических соединений.
- Производство пластмасс и резины: аммиак является важным компонентом в производстве синтетических пластмасс и резины. Он используется для синтеза основных сырьевых материалов, таких как мочевина и меламин.
- Холодильная техника: аммиак используется в промышленных холодильных системах, таких как холодильники и кондиционеры. Благодаря своей высокой холодильной способности и отсутствию вредного воздействия на окружающую среду, аммиак является эффективным и экологически безопасным веществом для охлаждения.
- Очистка воды: аммиак используется для очистки воды от загрязнений. Он может быть использован для устранения железа и марганца из воды, а также в процессах обеззараживания воды.
- Производство взрывчатых веществ: аммиак используется в производстве взрывчатых веществ, таких как тротил и аммиачное динамитное вещество. Он может служить источником азота и водорода для реакций в процессе синтеза этих веществ.
Это лишь некоторые примеры применения аммиака в промышленности. Благодаря своим химическим и физическим свойствам аммиак является ценным компонентом в различных отраслях промышленности.
Влияние аммиака на окружающую среду
Аммиак является естественным компонентом окружающей атмосферы. Он входит в состав отходов животного и растительного происхождения, а также используется во многих процессах в сельском хозяйстве и промышленности.
Выбросы аммиака могут приводить к загрязнению водных ресурсов. При попадании в атмосферу аммиак может оседать на поверхности воды и проникать в водные экосистемы. Это может привести к изменениям в планктонных сообществах и нарушению экологического баланса в водных экосистемах.
Аммиак является азотистым удобрением. Он используется в сельском хозяйстве для удобрения почвы и стимулирования роста растений. Однако, неправильное использование и избыточное применение аммиака могут привести к перегрузке почвы азотом и загрязнению водных ресурсов нитратами.
Аммиак может быть вовлечен в образование смога и воздушных загрязнений. Он взаимодействует с другими веществами в атмосфере и может способствовать образованию PM2.5 - мелкодисперсной аэрозольной частицы, которая является опасным загрязнителем воздуха и может приводить к проблемам с дыханием и сердечно-сосудистой системой.
Аммиак является важным компонентом в процессах очистки отходов и обезвреживания отходов. Он широко применяется в стационарных и мобильных системах очистки сточных вод, а также в процессах обезвреживания отходов. Аммиак может быть использован для превращения опасных веществ в безопасные соединения и обеспечения безопасной утилизации отходов.
Меры безопасности при работе с аммиаком

При работе с аммиаком необходимо соблюдать определенные меры безопасности, поскольку этот химический соединение может быть опасным при неправильном обращении. Вот некоторые важные предосторожности и меры безопасности:
1. Используйте защитные средства: Носите защитные очки, резиновые перчатки и халат, чтобы защитить глаза, кожу и одежду от контакта с аммиаком. Это поможет предотвратить возможные ожоги или раздражение.
2. Работайте в хорошо проветриваемом помещении: Аммиак имеет резкий и раздражающий запах. При работе с ним следует обеспечить хорошую вентиляцию, чтобы избежать вдыхания высоких концентраций этого вещества.
3. Избегайте непосредственного контакта с кожей и глазами: В случае попадания аммиака на кожу немедленно промойте его большим количеством воды. Если аммиак попал в глаза, следует промыть их водой не менее 15 минут и немедленно обратиться к врачу.
4. Храните аммиак в безопасном месте: Храните аммиак в плотно закрытых контейнерах в прохладном и сухом месте, вдали от источников огня и тепла. Это поможет предотвратить возможные взрывы или пожары.
5. Не смешивайте аммиак с другими химическими веществами: Аммиак может быть реактивным и может образовывать опасные смеси с некоторыми другими веществами. Поэтому следует строго соблюдать инструкции по безопасности и не смешивать аммиак с другими веществами без необходимости и соответствующих знаний.
Соблюдение этих мер безопасности поможет предотвратить возможные несчастные случаи и обеспечит безопасную работу с аммиаком.








