Ионный вид уравнения представляет собой способ записи химической реакции, в котором отображаются ионы, участвующие в этой реакции. В химии ионы являются заряженными атомами или молекулами, которые формируются в процессе химических реакций.
Ионный вид уравнения может быть использован для более точного отображения происходящих процессов в реакции. Он позволяет увидеть, какие конкретные ионы участвуют в реакции, и как происходит образование новых соединений.
Определение ионного вида уравнения осуществляется путем разделения на положительные и отрицательные ионы. Положительные ионы представляют катионы, или атомы с положительным ионным зарядом, а отрицательные ионы - анионы, или атомы с отрицательным ионным зарядом. В ионном виде уравнение записывается в виде совокупности ионов, с указанием их заряда и коэффициентов перед ними.
Пример ионного вида уравнения: NaCl + AgNO3 = AgCl + NaNO3
В данном примере ионного вида уравнения видно, что происходит образование агрегатов ионов Na+, Cl-, Ag+, NO3-. Это позволяет точно увидеть, какие ионы реагируют между собой и какие соединения образуются в результате реакции.
Понятие ионного вида уравнения

Ионный вид уравнения представляет собой способ записи химической реакции с использованием ионов. Химическая реакция в ионном виде показывает, какие ионы участвуют в процессе и какие ионы образуются.
Для записи химической реакции в ионном виде необходимо разделить все химические соединения на ионы, представляющиеся в растворе. Такие химические соединения, как кислоты, основания и соли, разделяются на ионы и записываются в ионном виде.
К примеру, реакция между хлоридом натрия (NaCl) и серной кислотой (H2SO4) может быть записана в ионном виде следующим образом:
| Ионный вид уравнения |
|---|
| Na+ + Cl- + 2H+ + SO42- → 2Na+ + 2Cl- + H2O + SO42- |
Таким образом, ионный вид уравнения позволяет более наглядно представить, какие ионы участвуют в реакции и какие новые соединения образуются.
Как определить ионный вид уравнения
Определение ионного вида уравнения позволяет выделить ионы, которые присутствуют в реакции. Для этого можно использовать несколько методов и подходов.
1. Анализ реагентов и продуктов реакции. Ионы могут быть получены из химических соединений путем диссоциации на положительные и отрицательные ионы. Например, соль NaCl диссоциирует на ионы Na+ и Cl-. Таким образом, уравнение реакции может содержать ионы Na+ и Cl-.
2. Запись уравнения реакции в ионной форме. В этом случае уравнение реакции записывается с использованием ионных символов. Например, вместо записи HCl + NaOH → NaCl + H2O можно записать H+ + Cl- + Na+ + OH- → Na+ + Cl- + H2O. При таком подходе все присутствующие в реакции ионы будут явно указаны.
3. Использование специальных методов анализа, таких как спектроскопия или хроматография. Эти методы позволяют идентифицировать ионы, присутствующие в реакции, по их спектральным или хроматографическим характеристикам.
Сочетание этих методов может помочь определить ионный вид уравнения и выделить основные ионы, участвующие в реакции.
Какие ионы присутствуют в ионном виде
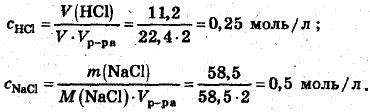
В ионном виде присутствуют ионы, которые образуются из неорганических и органических соединений. Например, ионы металлов и анионы, состоящие из одного атома или группы атомов. Формула ионов указывается в ионном виде с помощью знаков "+" и "-" для указания заряда.
Примеры ионов, которые могут присутствовать в ионном виде, включают:
- Катионы: калий (K+), натрий (Na+), магний (Mg2+), аммоний (NH4+) и др.
- Анионы: гидроксид (OH-), хлорид (Cl-), нитрат (NO3-), сульфат (SO42-) и др.
Знание ионного вида уравнения позволяет лучше понимать происходящие химические превращения и проводить анализ химических реакций.
Примеры уравнений с ионным видом
Ионный вид уравнения представляет собой запись реакции в виде ионов, а не молекул. Возможность разделения соединений на ионы позволяет упростить и анализировать химические реакции. Вот несколько примеров уравнений с ионным видом:
1. Реакция образования меди(II) оксида:
2Cu2+(aq) + O2-(aq) → 2CuO(s)
2. Реакция растворения хлорида натрия в воде:
NaCl(s) → Na+(aq) + Cl-(aq)
Здесь NaCl (иярид натрия) разделяется на натриевые ионы (Na+) и ионы хлора (Cl-) в растворе.
3. Реакция образования сульфата меди(II):
CuCO3(s) + H2SO4(aq) → CuSO4(aq) + CO2(g) + H2O(l)
4. Реакция образования серебра нитратом натрия:
AgNO3(aq) + NaCl(aq) → AgCl(s) + NaNO3(aq)
Здесь AgNO3 (нитрат серебра) разделяется на ионы серебра(Ag+), ионы натрия (Na+) и ионы нитрата(NO3-) в растворе.
Значение ионного вида уравнения для химической реакции

Ионный вид уравнения особенно полезен для анализа реакции и определения степени окисления атомов. Он позволяет более подробно изучить динамику происходящих процессов и идентифицировать все вещества, участвующие в реакции.
Чтобы записать уравнение в ионном виде, необходимо учитывать, что все катионы и анионы должны быть представлены отдельно, а заряд каждого иона должен быть указан в виде верхнего индекса справа от химического символа.
Например, химическая реакция, в которой хлорид натрия (NaCl) взаимодействует с серной кислотой (H2SO4), может быть записана в следующем ионном виде:
Na+ + Cl- + 2H+ + SO42- -> Na+ + Cl- + 2H2O + SO42-
В данном случае, ионный вид уравнения позволяет увидеть все ионы, которые образуются и участвуют в реакции. Он также позволяет легче анализировать изменение степени окисления атомов веществ и определять их реакционную способность.
Ионный вид уравнений в химической номенклатуре
Химическая реакция представляет собой процесс превращения одних химических веществ в другие при изменении их атомных строений. В ионном виде уравнение позволяет описать, как ионы одного вещества вступают во взаимодействие с ионами других веществ.
В ионном виде уравнения каждый ион записывается со своим зарядом и числом. Ионы, имеющие положительный заряд, называются катионами, а ионы с отрицательным зарядом - анионами. Ионы различаются по заряду и химическим элементам, к которым они принадлежат.
Для записи ионного вида уравнения используются следующие правила:
- Катионы записываются с положительным зарядом, а анионы - с отрицательным зарядом.
- Заряд каждого иона указывается в верхнем индексе.
- Число ионов каждого вида указывается внизу.
Пример ионного вида уравнения:
Na+(aq) + Cl-(aq) → Na+(aq) + Cl-(aq)
В данном примере ионы натрия (Na+) и ионы хлора (Cl-) представлены с указанием их зарядов и количества вещества.
Ионный вид уравнения позволяет более точно описать процессы, происходящие в химической реакции, и использовать его для расчетов концентраций ионов в растворах.








