Октет электронов – это важное понятие в химии, которое отражает фундаментальное стремление атомов некоторых элементов наряду с другими электронными окрестностями к аттракции идеальной конфигурации внешней оболочки семи самых высокоэнергетических электронов для каждого атома. В свою очередь, этот феномен определяет множество химических свойств элементов, их способность образовывать связи и участвовать в химических реакциях.
Ключевая роль октета электронов заключается в том, что атомы некоторых элементов стремятся достичь полной заполненности внешней электронной оболочки, содержащей восемь электронов. Этот октет стабилизирует атом, что приводит к устойчивости и возможности образования химических связей. Октет возникает, когда атом обладает восемью электронами в своей внешней электронной оболочке, что включает в себя два электрона s-полоски и шесть электронов p-полоски.
Интересно отметить, что октет электронов регулирует не только процессы образования и разрушения связей между атомами, но и законы электростатики. Его применение позволяет объяснить множество химических явлений, таких как образование ионов, силы межмолекулярного взаимодействия и реакционную способность.
Таким образом, октет электронов имеет принципиальное значение в химии. Он определяет химическую активность и реакционную способность элементов. Понимание и использование этого концепта является важным фактором в изучении и предсказании органических и неорганических реакций, а также в разработке новых материалов и лекарств.
Октет электронов в химии: его важность и роль
Октет электронов относится к наличию или достижению внешней оболочки атома восеми электронов, что приводит к устойчивости атома.
Октет электронов реализуется через различные типы химических связей. В основном, октет электронов связывается с атомами других элементов, чтобы достичь более устойчивого состояния.
Реакциями образования и разрыва химических связей атомы стремятся достичь октета электронов. При этом атомы обменают, передают или делят электроны, чтобы сформировать новые соединения.
В реакциях образования химических связей атомы могут достигнуть октета электронов, образуя ионическую связь, ковалентную связь или металлическую связь. Ионическая связь образуется между ионами с противоположными зарядами, ковалентная связь образуется через обмен электронами, а металлическая связь образуется в металлах, где электроны свободно передвигаются между атомами.
Реакции, в которых идет разрыв химической связи, происходят через образование или разрывание ковалентной связи. В таких реакциях атомы могут получить или потерять электроны, чтобы достичь октета электронов.
Октет электронов также влияет на физические свойства веществ, такие как температура кипения, температура плавления и растворимость. Например, вещества с более полностью заполненным октетом электронов обычно имеют более высокую температуру плавления и кипения.
В заключение, понимание октета электронов является важным для объяснения химических связей и реакций. Октет электронов помогает атомам достичь более устойчивого состояния и формировать стабильные химические соединения.
Значение октета электронов
Октет электронов представляет собой состояние атома, в котором его внешняя электронная оболочка содержит 8 электронов. Октетный окрашиватель представляет собой стремление атомов к достижению этого стабильного состояния путем приобретения, потери или обмена электронов с другими атомами.
Значение октета электронов в химии невероятно важно, поскольку атомы стремятся достичь октетного состояния, чтобы стабилизировать свою электронную оболочку. Достижение октетного состояния позволяет атому быть электронейтральным и обладать минимальной энергией. В результате этого желания атомы образуют химические связи с другими атомами, чтобы разделить, передать или приобрести электроны и достичь октета.
Октет электронов играет ключевую роль в химических реакциях и формировании химических связей между атомами. Это объясняет, почему атомы образуют ионы, вещества образуют ковалентные связи и молекулы существуют в газообразном, жидком или твердом состоянии. Знание о значении октета электронов помогает понять механизмы химических реакций, предсказывать свойства соединений и создавать новые материалы с желательными свойствами.
В заключение, октет электронов играет фундаментальную роль в химии, определяя химические связи, стабильность и свойства соединений. Понимание его значения позволяет более глубоко изучать и объяснять различные аспекты химических реакций и взаимодействий атомов веществ.
Формирование октета электронов
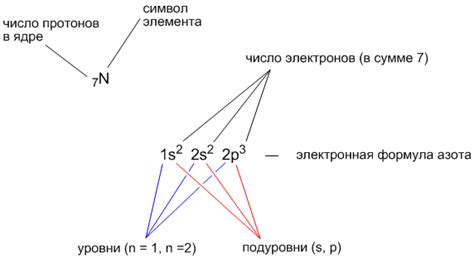
Атомы стремятся достичь октета электронов, чтобы установить стабильное состояние, похожее на состояние инертных газов. Для этого атомы могут образовывать химические связи с другими атомами. Существуют различные пути, по которым атомы достигают октета электронов.
1. Передача электронов: Атом с более низкой электроотрицательностью может передать один или несколько электронов атому с более высокой электроотрицательностью. Таким образом, оба атома достигают октета электронов.
2. Общие электронные пары: Два атома могут образовать химическую связь, в результате которой оба атома делят общие электронные пары. Таким образом, каждый атом получает дополнительные электроны и достигает октета электронов.
3. Деление электронных пар: Атомы могут делить общие электронные пары, перемещая их таким образом, чтобы каждый атом получал определенное количество электронов. Это позволяет атомам достичь октета электронов.
Формирование октета электронов играет ключевую роль в образовании различных химических соединений, таких как ионные соединения и молекулярные соединения. Оно обеспечивает стабильность и прочность связей атомов в химических соединениях.
Успешное формирование октета электронов позволяет атомам образовывать более стабильные соединения и химические связи, что является основой для многих химических реакций и химической активности веществ.
Роль октета электронов в химических реакциях
Имея полный октет электронов, атом становится стабильным и имеет меньшую склонность к химическим реакциям. Это связано с тем, что атомы нестабильных элементов стремятся достичь конфигурации инертного газа, чтобы уменьшить потенциальную энергию системы. Во время химических реакций атомы обменивают, снимают или принимают электроны, чтобы достичь состояния октетности.
Важной ролью октета электронов в химических реакциях является обеспечение стабильности соединений и формирование ковалентных и ионных связей. В химической связи атомы обменивают или делят электроны, чтобы достичь октета в своих внешних оболочках. Обычно это происходит путем образования ковалентных связей, где электроны обмениваются парами.
Если атом не имеет октета в своей внешней оболочке, он будет стремиться найти или отдать электроны, чтобы достичь этого состояния, избегая тем самым нестабильности. Нестабильные атомы обладают большей электроотрицательностью и имеют большую склонность к химическим реакциям, а также могут проявлять свойства окислителей или восстановителей.
В заключение, октет электронов играет важную роль в химических реакциях, обеспечивая стабильность атомов и формирование химических связей. Многие свойства и реакции веществ связаны с достижением октета электронов внешней оболочки атома.








