Неспаренные электроны являются одиночными электронами, которые находятся на атомах внешней оболочки. Обычно все электроны на внешней оболочке атома образуют пары. Но в некоторых случаях может возникнуть ситуация, когда атом имеет один или более электронов без пары. Эти неспаренные электроны играют важную роль в химических реакциях и оказывают влияние на свойства вещества.
Неспаренные электроны обладают высокой химической активностью, так как они стремятся образовать пары со свободными электронами других атомов, чтобы достичь более устойчивого состояния. Это объясняет, почему атомы с неспаренными электронами обладают возможностью образовывать химические связи и участвовать в реакциях с другими атомами.
Неспаренные электроны в химии играют важнейшую роль в образовании химических связей, структуре молекул и свойствах вещества.
Неспаренные электроны могут образовывать связи с другими атомами и молекулами, что приводит к образованию новых соединений и возникновению новых свойств. Также неспаренные электроны могут вступать в реакции с электронами других атомов, образуя химические связи и меняя структуру молекулы.
Важным свойством неспаренных электронов является их способность взаимодействовать с определенными видами электромагнитного излучения. Это явление используется в химическом анализе и спектроскопии для определения состава вещества и изучения его структуры.
Как неспаренные электроны влияют на химические реакции?
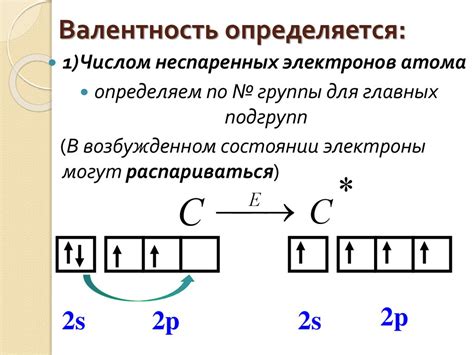
В химии неспаренными электронами называются электроны, находящиеся на внешнем электронном уровне атома и не образующие пары с другими электронами. Неспаренные электроны обладают незанятыми электронными орбиталями, что делает их особенно активными и влияющими на химические реакции.
Одна из основных ролей неспаренных электронов в химических реакциях - участие в образовании химических связей. Неспаренные электроны могут образовывать связи с другими атомами или ионами путем обмена электронами или обобщения электронных облаков. Таким образом, они могут участвовать в образовании молекул и кристаллических решеток.
Неспаренные электроны также могут служить возможной точкой прикрепления других частиц, таких как ионы или молекулы. Это может привести к образованию новых химических соединений или реакций с уже существующими соединениями. Такое взаимодействие играет важную роль в металлоорганической химии и катализе.
Неспаренные электроны способны образовывать беспроводные пары электронов и обладают уникальными свойствами, которые позволяют им образовывать связи с атомами других элементов. Это позволяет неспаренным электронам влиять на структуру и стабильность соединений.
Самые распространенные элементы, имеющие неспаренные электроны, это кислород (O), азот (N), сера (S), фтор (F), фосфор (P) и хлор (Cl). Комплексы с неспаренными электронами могут проявлять особые свойства, такие как химическая реактивность, магнитные свойства и свойства катализаторов.
Таким образом, неспаренные электроны играют важную роль в химических реакциях, обеспечивая возможность образования новых связей и соединений. Их уникальные свойства и взаимодействия позволяют электронам участвовать в различных процессах, от реакций с образованием новых соединений до катализа и стабилизации химических систем.
Что такое неспаренные электроны в химии?
Роль неспаренных электронов в структуре атома

Неспаренные электроны определяют химическую активность атомов. Их наличие делает атомы более реакционноспособными и склонными к образованию химических связей с другими атомами. Неспаренные электроны могут участвовать в обмене или совместном использовании с другими атомами, образуя химические связи.
Неспаренные электроны также определяют форму и размеры атомов. Они обладают электростатическими свойствами, которые определяют взаимное расположение атомов в молекуле. Неспаренные электроны могут отталкиваться или притягиваться друг к другу и к другим атомам, что влияет на структуру и свойства молекулы. При этом они создают электронные облака, формирующие пространственную структуру атомов.
Кроме того, неспаренные электроны могут участвовать в обменных взаимодействиях с другими атомами. Они могут притягивать электроны от других атомов или отдавать свои электроны, что приводит к образованию связей между атомами. Это позволяет атомам образовывать сложные молекулы с различными свойствами и функциями.
Таким образом, неспаренные электроны играют важную роль в структуре атома, определяющую его свойства и поведение в химических реакциях. Их наличие влияет на химическую активность атомов, форму и размеры атомов, а также на возможность образования химических связей и молекул. Понимание роли неспаренных электронов помогает нам лучше понять химические реакции и свойства вещества.
Как неспаренные электроны взаимодействуют с другими атомами?
Взаимодействие неспаренных электронов с другими атомами имеет особое значение в химических реакциях. Неспаренные электроны могут быть использованы для образования новых химических связей.
Когда атом с неспаренными электронами встречает атом с несвязанными электронными парами, происходит химическая реакция. Неспаренные электроны атакуют электронную пару, образуя новую связь между атомами.
Также, неспаренные электроны могут привлекать электроноотрицательные атомы и образовывать так называемые диполь-дипольные связи. Взаимодействие неспаренных электронов с электронными парами также может приводить к образованию радикалов, которые имеют большую реакционную активность.
Взаимодействие неспаренных электронов с другими атомами в химических реакциях играет ключевую роль в образовании новых веществ и изменении структуры молекул. Это является основой для понимания множества химических процессов и разработки новых соединений с желаемыми свойствами.
| Примеры химических реакций с участием неспаренных электронов: |
|---|
| 1. Реакция радикального замещения, где радикал с неспаренным электроном замещает атом или группу атомов в молекуле. |
| 2. Образование координационных соединений, где неспаренные электроны атома металла образуют связь с электронными парами атома лиганда. |
| 3. Реакция аддиции, где неспаренные электроны атома присоединяются к молекуле и образуют новую связь. |
| 4. Электронный перенос, где неспаренные электроны передаются от одного атома к другому, образуя новые связи. |








